一、鎖志剛(哈佛大學(xué))
擠出打印是一種很有前途的快速成型方法,但現(xiàn)有的方法不能滿足基本要求:打印水凝膠和彈性體的整體結(jié)構(gòu),按任意順序,具有很強的附著力。對此問題,哈佛大學(xué)鎖志剛教授團(tuán)隊與西安交通大學(xué)唐敬達(dá)實驗室合作共同提出一種軟結(jié)構(gòu)3D打印的強韌粘接技術(shù),實現(xiàn)了具有超強界面粘接的水凝膠/彈性體親疏水異質(zhì)結(jié)構(gòu)的打印1。
圖1-打印水凝膠和彈性體整體結(jié)構(gòu)的方法示意圖
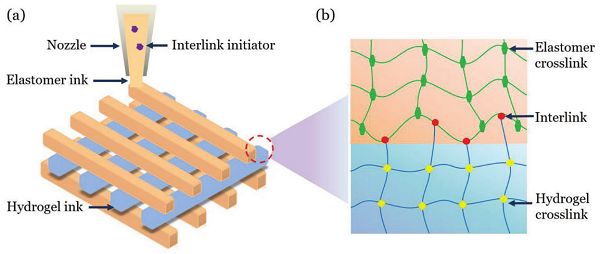
研究人員將聯(lián)接引發(fā)劑溶于彈性體材料中,分別調(diào)節(jié)彈性體預(yù)聚液和水凝膠預(yù)聚液的粘度,將兩者以任意順序3D打印在一起,然后引發(fā)聚合反應(yīng),形成具有強韌粘接的水凝膠/彈性體復(fù)合體。該方法不同于常用的表面改性,采用本體改性的策略,可為可拉伸器件、軟機(jī)器制備以及其它異質(zhì)材料的復(fù)合3D打印提供一種通用的解決方法,如圖1。即在印刷打印過程中,每一種材料的墨水都在壓力梯度下流過噴嘴,但在重力和毛細(xì)作用下仍能保持形狀。固化過程中形成共價鍵,將單體單元連接成聚合物鏈,將聚合物鏈交聯(lián)到水凝膠和彈性體的聚合物網(wǎng)絡(luò)中,并將兩個聚合物網(wǎng)絡(luò)連接成一個整體結(jié)構(gòu)。該方法通過在其中一種油墨中添加一種鏈接引發(fā)劑,將水凝膠網(wǎng)絡(luò)和彈性體網(wǎng)絡(luò)共價連接起來。黏附能在5000 J /m 2以上。打印出來的變形結(jié)構(gòu)能夠經(jīng)受住腫脹,而打印出來的人造軸突能夠經(jīng)受住錘子的反復(fù)擊打。這種方法為開發(fā)廣泛應(yīng)用于醫(yī)學(xué)和工程的軟設(shè)備開辟了道路。研究團(tuán)隊將相關(guān)研究成果以“Printing Hydrogels and Elastomers in Arbitrary Sequence with Strong Adhesion”為題發(fā)表在國際著名期刊Advanced Functional Materials上。
柔性可拉伸材料(高彈體、凝膠等)在可拉伸電子器件、軟體機(jī)器人、藥物釋放和組織再生等領(lǐng)域有著廣泛的應(yīng)用前景。大多數(shù)應(yīng)用場景需要可拉伸材料具有低滯后性和高韌性--即材料在正常工作范圍內(nèi)的拉伸和恢復(fù)過程中耗散較少的能量,當(dāng)出現(xiàn)裂紋時在裂紋尖端區(qū)域耗散較多的能量以阻止裂紋的擴(kuò)展。但是,材料的韌性和滯后性通常具有正相關(guān)性,從而不能同時滿足以上要求。例如,單聚合物網(wǎng)絡(luò)的高彈性彈性體或水凝膠具有低滯后和低韌性。單一網(wǎng)絡(luò)通常通過添加填料或者加入第二層網(wǎng)絡(luò)引入犧牲鍵來增韌,但犧牲鍵的斷裂和重建可能會導(dǎo)致明顯的滯后。從而使其無法應(yīng)用到軟體機(jī)器人、傳感器和制動器等器件中。并且不管引入的犧牲鍵是否能自修復(fù),這一類韌性材料的疲勞閾值都遠(yuǎn)低于其斷裂韌性。
圖2-具有不同網(wǎng)絡(luò)結(jié)構(gòu)的可拉伸材料的韌性和滯后性

針對這一問題,美國哈佛大學(xué)鎖志剛教授團(tuán)隊提出了一種打破韌性和滯后相關(guān)性,同時實現(xiàn)高韌性和低滯后性的設(shè)計原理2。利用這一工作原理,通過制備低彈性模量基體和高彈性模量纖維的復(fù)合材料,它破壞了韌性與滯后的關(guān)系,實現(xiàn)了高韌性和低滯后。復(fù)合材料保留了較低的滯后,但是具有較高的韌性(10000 J/m2)和抗疲勞性能。通過實驗和計算,確定了大模量對比降低了裂紋前沿的應(yīng)力集中,強附著力使纖維與基體結(jié)合,抑制了纖維與基體之間的滑移。高韌性、低滯后的可拉伸材料為高循環(huán)、低功耗的軟機(jī)器人和軟人機(jī)界面的創(chuàng)造提供了機(jī)會。如圖2,在裂紋尖端,纖維和基體的高模量比能顯著降低裂尖附近的應(yīng)力集中,使一大段纖維被高度拉伸。當(dāng)纖維斷裂時,整個高度拉伸區(qū)域內(nèi)的彈性能被釋放。這一過程類似于單一聚合物網(wǎng)絡(luò)的斷裂過程。但是在單一聚合物網(wǎng)絡(luò)中,只有裂尖的一層分子鏈被高度拉伸,當(dāng)裂紋擴(kuò)展時,存儲在這一層分子鏈中的彈性能被釋放。而復(fù)合材料中的高度拉伸區(qū)域的尺寸高出分子鏈長度數(shù)個數(shù)量級,從而實現(xiàn)高韌性。只要基體和纖維材料具有低滯后,并且界面粘接足夠強,合成的復(fù)合材料就能保持低滯后性。同時材料的抗疲勞性能也能得到顯著提升。研究團(tuán)隊將相關(guān)研究成果以“Stretchable materials of high toughness and low hysteresis”為題發(fā)表在國際著名期刊PNAS上。
近年來,水凝膠基軟器件得到了廣泛的發(fā)展。例如,軟機(jī)器人,類皮膚傳感器,可拉伸光纖,透明摩擦發(fā)電機(jī),和可拉伸電離能器件。這些應(yīng)用的工作條件涉及長時間的重復(fù)機(jī)械載荷,因此水凝膠不僅需要長時間維持其功能,而且需要長時間保持良好的機(jī)械強度和可拉伸性。但是,所有的水凝膠都存在不同程度的空洞、裂紋、雜質(zhì)等缺陷,易發(fā)生斷裂。由此,大多數(shù)堅韌的水凝膠都是通過吸收破壞犧牲鍵的巨大能量損耗而設(shè)計的。然而,這些水凝膠在長時間的循環(huán)載荷作用下仍然會斷裂,甚至出現(xiàn)小的裂紋。
圖3-制備了具有PVA晶體結(jié)構(gòu)的對缺陷不敏感的PAAm-PVA-S水凝膠

基于此,哈佛大學(xué)鎖志剛教授團(tuán)隊提出了靜載和循環(huán)載荷作用下對裂紋不敏感的水凝膠的工作原理。該設(shè)計使水凝膠中的聚合物鏈在分子水平上對齊,以偏轉(zhuǎn)裂紋3。為了證明這一原理,以聚丙烯酰胺和聚乙烯醇為原料,制備了一種晶域排列整齊的水凝膠,如圖3。當(dāng)水凝膠在準(zhǔn)直方向拉伸時,初始缺陷裂紋偏轉(zhuǎn),沿加載方向傳播,將材料剝離下來,水凝膠又變得完美無瑕。這種水凝膠對已經(jīng)存在的缺陷不敏感,即使在一萬多次加載循環(huán)下也不敏感。通過實驗和斷裂力學(xué)計算,確定了各向異性達(dá)到裂紋撓度的臨界程度。并且該原理可推廣到其它水凝膠體系。研究團(tuán)隊并將相關(guān)研究成果以“Flaw-Insensitive Hydrogels under Static and Cyclic Loads”為題發(fā)表在著名期刊Macromolecular Rapid Communication上。
二、趙選賀(麻省理工學(xué)院)
生物電子與人體的交互作用,包括電刺激和神經(jīng)活動的記錄,是神經(jīng)科學(xué)與工程、診斷、治療、可穿戴和可植入設(shè)備等領(lǐng)域快速發(fā)展的基礎(chǔ)。由于軟的、濕的和活的生物組織與硬的、干的和合成的電子系統(tǒng)之間的內(nèi)在差異,在這兩個不同領(lǐng)域之間開發(fā)更兼容、更有效和更穩(wěn)定的接口一直是科學(xué)和技術(shù)領(lǐng)域中最艱巨的挑戰(zhàn)之一。近年來,水凝膠因其與生物組織的相似性以及在電氣、機(jī)械和生物功能工程方面的多功能性,成為下一代生物電子界面的一種有前途的候選材料。
圖4-水凝膠可以在生物學(xué)和電子學(xué)之間架起橋梁,為生物電子學(xué)的應(yīng)用提供廣闊前景
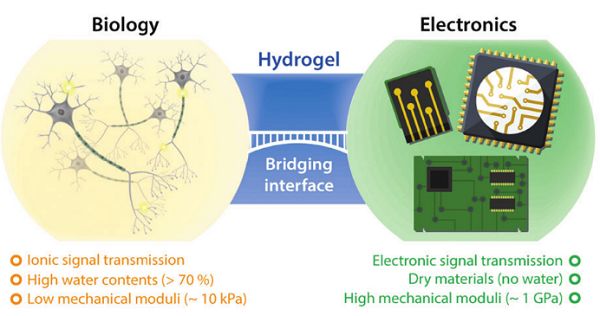
由此,麻省理工學(xué)院趙選賀研究團(tuán)隊首次提出水凝膠是人機(jī)界面的最理想載體之一,系統(tǒng)定義了水凝膠生物電子學(xué)的基本原理和材料設(shè)計原則,給出了現(xiàn)有的水凝膠電子材料的例子,并建議了水凝膠生物電子學(xué)未來發(fā)展的方向4。如圖4,論文中主要綜述了(i)組織-電極相互作用的基本機(jī)理,(ii)水凝膠與人體生物電氣界面的獨特優(yōu)勢,(iii)生物電子學(xué)水凝膠發(fā)展的最新進(jìn)展,以及(iv)未來水凝膠生物電子學(xué)設(shè)計的合理指南。水凝膠生物電子學(xué)的進(jìn)步將為生物學(xué)和電子學(xué)的緊密結(jié)合帶來前所未有的機(jī)遇,有可能模糊人類和機(jī)器之間的界限。研究團(tuán)隊將特邀綜述論文以“Hydrogel bioelectronics”為題發(fā)表在國際頂級期刊Chemical Society Reviews上。
在現(xiàn)代的醫(yī)療技術(shù)手段中,與生物體相互作用的裝置通常是由金屬、硅、陶瓷和塑料制成。而為了長期監(jiān)測或治療,植入此類設(shè)備通常是侵入性程序。這樣會給病人或醫(yī)生帶來相當(dāng)大的痛苦和麻煩。比如做胃鏡,有時甚至需要麻醉,如此給病人帶來極大的痛苦和傷害,并且這些通常的可服用器件大多受限于胃腸運轉(zhuǎn)時間,最多在消化道滯留1-2天,不能長期監(jiān)測體征。而水凝膠具有良好的機(jī)械順應(yīng)性和生物相容性,為人機(jī)交互提供了新的機(jī)遇。使用水凝膠來完成胃的駐留需要水凝膠膨脹得非常快,并且隨著時間的推移能夠承受胃的機(jī)械力。然而,現(xiàn)有的水凝膠中,高膨脹比、高膨脹速度和不具有長期保持強度的特點。
圖5-水凝膠器件的設(shè)計方案
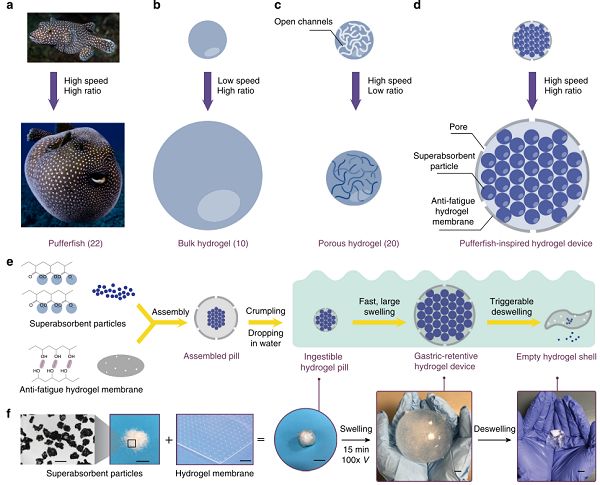
基于此,麻省理工學(xué)院趙選賀研究團(tuán)隊首次提出并實現(xiàn)可食用水凝膠電子設(shè)備,實現(xiàn)了吃一顆“果凍”,就可以長期監(jiān)控核心體征例如溫度、pH、進(jìn)食和吃藥情況、以及消化道病變30天5。研究團(tuán)隊的解決方案是根據(jù)河豚的啟發(fā),將水凝膠設(shè)計成膠囊型,如圖5,該膠囊由兩種材料的水凝膠組成。膠囊內(nèi)部是聚丙烯酸鈉,一種超吸水水凝膠顆粒,能夠?qū)崿F(xiàn)快速吸水和大體積溶脹。口服水凝膠膠囊只有一粒藥丸大小,口服后在胃中快速吸水膨脹體積100倍左右,能夠長期滯留在胃腔內(nèi)部。該水凝膠器件在胃中可以同時保持柔軟性和抗疲勞性:一方面,它能夠?qū)崿F(xiàn)與胃腔膜的柔性接觸,避免磨損胃腔,引起胃潰瘍等不良排異反應(yīng);另一方面,能夠長期抵抗胃腔的機(jī)械蠕動和胃酸的化學(xué)腐蝕。此外,通過在水凝膠中嵌入電子傳感器 (例如溫度傳感器),可以持續(xù)監(jiān)測核心體征(例如胃內(nèi)溫度)長達(dá)一個月。研究團(tuán)隊將相關(guān)研究成果以“Ingestible hydrogel device”為題發(fā)表在國際頂級期刊Nature Communications上。
長期穩(wěn)定高效的人機(jī)界面交互及融合過程中要求界面材料同時具備高電導(dǎo)率、優(yōu)異的穩(wěn)定性、良好的生物兼容性以及與人體組織匹配的力學(xué)性能。導(dǎo)電聚合物水凝膠是實現(xiàn)人體和生物電子設(shè)備完美兼容的理想界面材料之一,然而現(xiàn)有導(dǎo)電水凝膠很難兼顧滿足應(yīng)用需求的電學(xué)、力學(xué)、生物兼容性及穩(wěn)定性。 導(dǎo)電聚合物的水凝膠,特別是聚(3,4-乙二氧噻吩):聚苯乙烯磺酸鹽(PEDOT:PSS),由于其良好的電氣和機(jī)械性能,為傳感和刺激生物組織提供了一個有前途的電氣界面。
圖6-純(PEDOT:PSS)水凝膠的制備圖
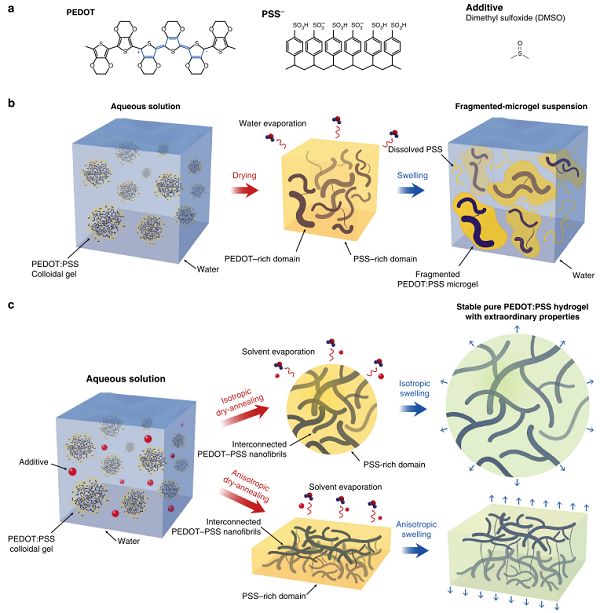
由此,麻省理工學(xué)院趙選賀研究團(tuán)隊提出形成穩(wěn)定的導(dǎo)電聚合物納米纖維互聯(lián)網(wǎng)絡(luò)是獲得高性能導(dǎo)電聚合物水凝膠的關(guān)鍵,同時發(fā)明了一種簡單有效的方法,用來設(shè)計高性能聚(3,4-亞乙二氧基噻吩):聚(苯乙烯磺酸鹽) (PEDOT:PSS)水凝膠6,如圖6。所報道的純PEDOT:PSS水凝膠電導(dǎo)率可達(dá)40 S/cm,力學(xué)性能良好(拉斷伸長率大于35%,楊氏模量2 MPa),同時具有良好的電學(xué)、電化學(xué)及力學(xué)穩(wěn)定性。純PEDOT:PSS導(dǎo)電水凝膠的制備有助于加深人們對高性能導(dǎo)電水凝膠合理設(shè)計的理解,優(yōu)越的機(jī)械、電氣和電化學(xué)穩(wěn)定性和可調(diào)濕的生理環(huán)境中各向同性和各向異性腫脹,為新一代生物電子產(chǎn)品制作及應(yīng)用提供了更佳的材料平臺。研究團(tuán)隊將相關(guān)研究成果以“Pure PEDOT:PSS hydrogels”為題發(fā)表在國際頂級期刊Nature Communications上。
水凝膠在設(shè)備和機(jī)器中的新應(yīng)用要求水凝膠在循環(huán)機(jī)械載荷下保持韌性和強度。當(dāng)水凝膠在單周機(jī)械載荷作用下能夠抵抗斷裂時,這些增韌凝膠在多周載荷作用下仍然會發(fā)生疲勞斷裂。水凝膠是人造軟骨、關(guān)節(jié)和椎間盤的理想替代材料。這些應(yīng)用要求水凝膠具備循環(huán)加載下的抗疲勞性能。現(xiàn)在報道的合成水凝膠的疲勞閾值在1到100 J/m2之間,因而設(shè)計具有抗疲勞斷裂的水凝膠仍是軟材料領(lǐng)域的一大難題。
圖7-抗疲勞斷裂水凝膠的設(shè)計原理
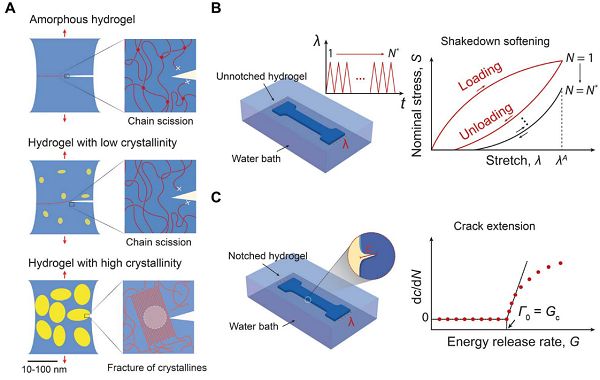
人體的韌帶肌肉大概每年承受幾百萬次兆帕級的應(yīng)力,并且保持疲勞閾值在1000 J/m2以上。韌帶肌肉中膠原蛋白的有序晶區(qū)可能是它們抗疲勞的原因。受生物組織啟發(fā),麻省工學(xué)院的趙選賀研究團(tuán)隊提出,設(shè)計抗疲勞斷裂水凝膠需要使單位面積能量的疲勞裂紋遇到斷裂能遠(yuǎn)高于一層聚合物鏈的物質(zhì)7。例如納米晶域等,如圖7。并研究證明,控制水凝膠中結(jié)晶度的引入可以顯著提高其抗疲勞斷裂性能。膨脹狀態(tài)下結(jié)晶度為18.9%的聚乙烯醇(PVA)疲勞閾值可超過1000 J/m2,抗疲勞設(shè)計原理可以用來指導(dǎo)開發(fā)具有長期使用價值的水凝膠設(shè)備和器械。研究團(tuán)隊并將相關(guān)研究成果以“Anti-fatigue-fracture hydrogels”為題發(fā)表在國際著名期刊Science Advances上。
三、江雷(中國科學(xué)院院士)維度異質(zhì)結(jié)構(gòu)體系中的范德華整合策略
隨著科技和社會的發(fā)展,海洋開發(fā)變得越來越必要和頻繁。在這一過程中,海洋生物污損現(xiàn)象十分嚴(yán)重,主要是指海洋生物在材料表面附著和聚集。從而帶來不利的影響。比如,會因此增大船只的阻力,導(dǎo)致航速下降,油耗增加;加速材料老化腐蝕等問題,其造成了的大量的經(jīng)濟(jì)損失。為了克服這些困難,已經(jīng)采取了許多措施。目前的海洋防污策略大部分還屬于無差別毒殺,不僅效率低,而且還可能導(dǎo)致毒物通過生物鏈富集再被人食用。因此,發(fā)展一種高效、環(huán)保的海洋防污方法仍是當(dāng)務(wù)之急。其中硅藻的粘附是海洋生物污染過程中的最嚴(yán)重的問題之一。
圖8-SOSA凝膠制備示意圖
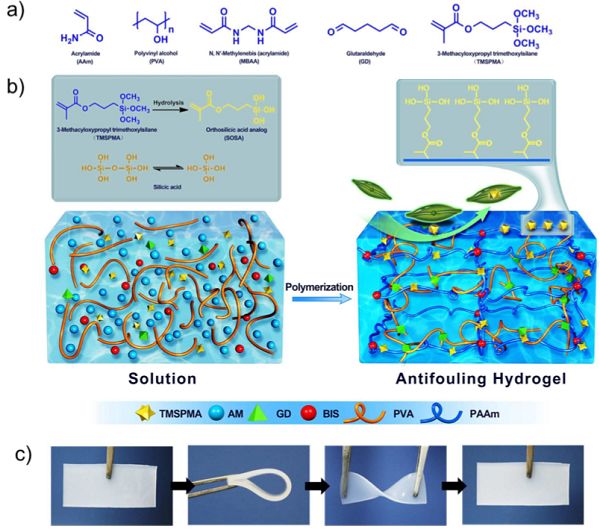
基于此,中科院理化所江雷院士研究團(tuán)隊和海南大學(xué)郝萬軍教授合作首次提出利用原硅酸類似物誘導(dǎo)硅藻攝取,進(jìn)而干擾硅藻正常的生命活動,最終實現(xiàn)抗硅藻附著8。由于硅藻合成二氧化硅外殼需要大量攝取硅酸,而人和其他海洋生物并不吸收硅酸。針對這一差異,研究團(tuán)隊使用一種人工合成的原硅酸類似物(SOSA),如圖8。3-甲基丙烯酰氧基丙基三甲氧基硅烷(TMSPMA),通過共聚固定在凝膠中并水解得到帶有三個硅羥基的SOSA,制得柔韌的抗硅藻附著凝膠。在水凝膠中,SOSA具有與原硅酸非常類似的三個Si-OH,并且還有一個在水中穩(wěn)定的C-Si鍵。當(dāng)這些物質(zhì)被凝膠表面的污損硅藻攝取之后,由于其中的C-Si鍵相對比較穩(wěn)定,不會像原硅酸一樣縮合形成二氧化硅外殼,所以硅藻的正常生命活動將出現(xiàn)紊亂,最終影響硅藻的附著行為。詳細(xì)研究表明,含SOSA的水凝膠具有良好的抗硅藻粘附性能,SOSA的抗硅藻作用是有針對性的,只有試圖粘附在SOSA水凝膠表面的生物體受到影響。SOSA水凝膠具有高效、環(huán)保的特性,在海洋防污方面具有廣闊的應(yīng)用前景。研究團(tuán)隊將相關(guān)研究成果以“Preventing diatoms adhesion using a hydrogel with orthosilicic acid analog as deceptive food”為題發(fā)表在國際著名期刊Journal of Materials Chemistry A上。
在生命體細(xì)胞信號的傳遞中,離子分布調(diào)控在生物轉(zhuǎn)變中是十分重要的。如維持細(xì)胞的離子平衡,信號轉(zhuǎn)導(dǎo)以及能量采集。納米通道門控機(jī)制可以通過各種觸發(fā)物質(zhì)來實現(xiàn)離子分布的調(diào)控,如pH、電壓、溫度以及光等的刺激都能實現(xiàn)控制離子或分子在人工離子通道中的傳輸及分布。近年來DNA納米技術(shù)發(fā)展迅速,特別是核酸在外界刺激下的可逆轉(zhuǎn)變響應(yīng)及其豐富的刺激源,使DNA納米技術(shù)十分適用于離子通道門控機(jī)制的實現(xiàn)。然而,由于DNA門控納米通道的單層結(jié)構(gòu)中存在少量的DNA基質(zhì),以及納米通道的尺寸較小,導(dǎo)致其離子轉(zhuǎn)運選擇性(整流比)和效率(離子通量)有限,這是近年來DNA門控納米通道研究的不足之處。此外,在現(xiàn)有的DNA納米通道中,陰陽離子傳輸?shù)姆较虿⒉荒艿玫娇刂啤R虼耍瑸榱颂岣逥NA納米通道中離子傳輸能力,實現(xiàn)可重構(gòu)的DNA結(jié)構(gòu)設(shè)計是必要的。
圖9-離子通道制備過程以及DNA水凝膠網(wǎng)絡(luò)形成和過渡過程示意圖
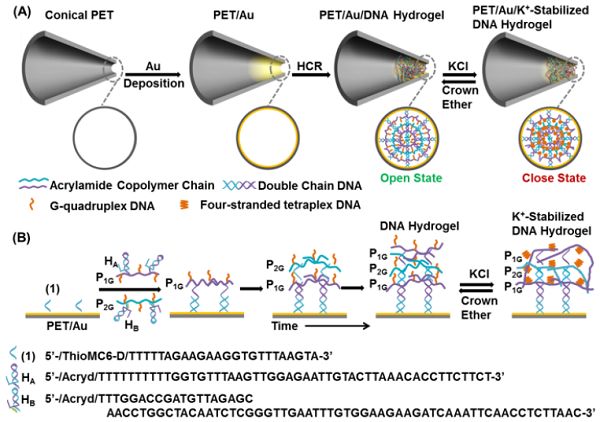
由此,中科院理化所江雷院士團(tuán)隊和北化所的田野副研究員以及以色列耶路撒冷希伯來大學(xué)的I. Willner教授合作首次開發(fā)了基于智能DNA水凝膠刺激響應(yīng)的離子通道9,如圖9。DNA水凝膠是一種具有空間負(fù)電荷的三維網(wǎng)絡(luò)結(jié)構(gòu),與納米通道中存在的其他響應(yīng)分子不同,其離子通量和整流比均有顯著提高。通過K+離子和冠醚的循環(huán)處理,DNA水凝膠狀態(tài)可以在剛性較差的網(wǎng)絡(luò)和剛性較差的網(wǎng)絡(luò)之間可逆切換,從而提供了納米通道的門控機(jī)制。基于DNA水凝膠的結(jié)構(gòu)和pH刺激,可以精確控制陽離子或陰離子的轉(zhuǎn)運方向,實現(xiàn)多個門控特性。同時,水凝膠中的G-quadruplex DNA(G-quadruplex 四聯(lián)體,是一種由富含鳥嘌呤的核酸序列所構(gòu)成的四股型態(tài))可能被其他刺激反應(yīng)性DNA分子、肽或蛋白質(zhì)所取代,這為智能水凝膠提高納米通道的功能開辟了一條新的途徑。研究團(tuán)隊將相關(guān)研究成果以“Smart DNA Hydrogels Integrated Nanochannels with High Ion Flux and Adjustable Selective Ionic Transport”為題發(fā)表在國際頂級期刊Angewandte Chemie-International Edition上。
參考文獻(xiàn)
1.Yang, H.; Li, C.; Yang, M.; Pan, Y.; Yin, Q.; Tang, J.; Qi, H. J.; Suo, Z., Printing Hydrogels and Elastomers in Arbitrary Sequence with Strong Adhesion. Advanced Functional Materials 2019, 1901721.
2.Wang, Z.; Xiang, C.; Yao, X.; Le Floch, P.; Mendez, J.; Suo, Z., Stretchable materials of high toughness and low hysteresis. Proceedings of the National Academy of Sciences of the United States of America 2019,116(13), 5967-5972.
3.Bai, R.; Yang, J.; Morelle, X. P.; Suo, Z., Flaw-Insensitive Hydrogels under Static and Cyclic Loads. Macromol Rapid Commun 2019, e1800883.
4.Yuk, H.; Lu, B.; Zhao, X., Hydrogel bioelectronics. Chemical Society reviews 2019,48(6), 1642-1667.
5.Liu, X.; Steiger, C.; Lin, S.; Parada, G. A.; Liu, J.; Chan, H. F.; Yuk, H.; Phan, N. V.; Collins, J.; Tamang, S.; Traverso, G.; Zhao, X., Ingestible hydrogel device. Nature communications 2019,10(1), 493.
6.Lu, B.; Yuk, H.; Lin, S.; Jian, N.; Qu, K.; Xu, J.; Zhao, X., Pure PEDOT:PSS hydrogels. Nature communications 2019,10(1), 1043.
7.Shaoting Lin, Xinyue Liu, Ji Liu, Hyunwoo Yuk, Hyun-Chae Loh, German A. Parada, Charles Settens, Jake Song, Admir Masic, Gareth H. McKinley, Xuanhe Zhao., ScienceAdvances. 2019;5 : eaau8528.
8.Chen, W.; Hao, D.; Guo, X.; Hao, W.; Jiang, L., Preventing diatom adhesion using a hydrogel with an orthosilicic acid analog as a deceptive food. Journal of Materials Chemistry A 2018,6(39), 19125-19132.
9.Wu, Y.; Wang, D.; Willner, I.; Tian, Y.; Jiang, L., Smart DNA Hydrogel Integrated Nanochannels with High Ion Flux and Adjustable Selective Ionic Transport. Angew Chem Int Ed Engl 2018,57(26), 7790-7794.
免責(zé)聲明:本網(wǎng)站所轉(zhuǎn)載的文字、圖片與視頻資料版權(quán)歸原創(chuàng)作者所有,如果涉及侵權(quán),請第一時間聯(lián)系本網(wǎng)刪除。

官方微信
《中國腐蝕與防護(hù)網(wǎng)電子期刊》征訂啟事
- 投稿聯(lián)系:編輯部
- 電話:010-62313558-806
- 郵箱:fsfhzy666@163.com
- 中國腐蝕與防護(hù)網(wǎng)官方QQ群:140808414





