1. 基于水凝膠響應壓力梯度直接產生離子電流
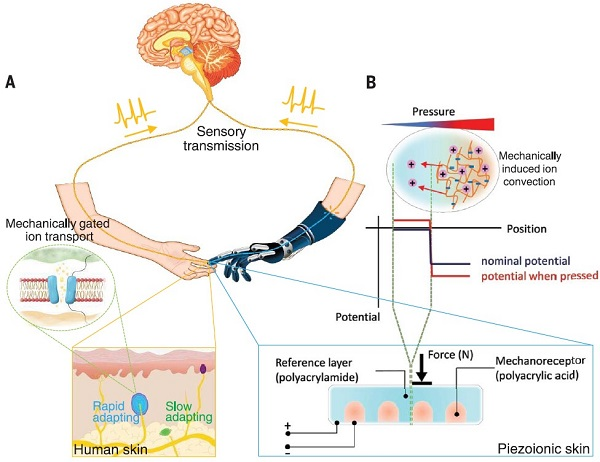
加拿大英屬哥倫比亞大學的John D. W. Madden(通訊作者)等人提出了一種離子型壓電方法,可基于水凝膠響應壓力梯度直接產生離子電流(即離子壓電效應,piezoionic effect)。在該研究所設計制備的水凝膠中,陽離子和陰離子的遷移行為不同,因此當被擠壓時水凝膠可形成離子梯度并產生電壓。由此產生的離子電流具有變化范圍較寬的持續時間(從毫秒級別到數百秒級別),并且可發揮直接的神經調節和肌肉興奮作用。陽離子和陰離子的遷移差異還可決定信號放大程度和持續時間,而同時,具有固定電荷梯度的圖案化水凝膠薄膜可提供接近細胞電位的電壓補償,因此結合這兩種效應,研究創造的自供能超軟離子壓電機械感受器可產生比摩擦納米發電和壓電器件高4-6個數量級的電荷密度,有望為設計仿生感知接口提供新的思路。本文第一作者為Yuta Dobashi,研究成果以題為“Piezoionic mechanoreceptors: Force-induced current generation in hydrogels”發表在國際著名期刊Science上。
2. 雙重信息加密功能的熒光油/水凝膠
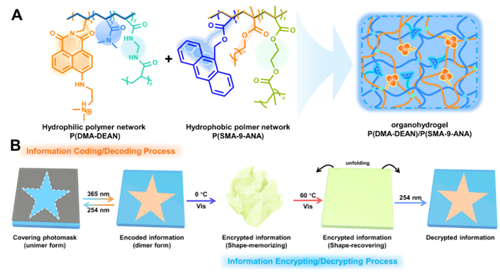
據中國科學院寧波材料技術與工程研究所官網報道,智能高分子材料團隊在陳濤研究員的帶領下,在熒光水凝膠體系的構建及其顏色調控與動態信息防偽方面取得了一系列的研究進展。近期,陳濤研究員、樂曉霞副研究員報道了他們最新的在具有雙重信息加密功能的熒光油/水凝膠方面的科研工作。該油/水凝膠由互穿的水凝膠和油凝膠聚合物網絡組成,其中萘酰亞胺基團(DEAN,發射黃綠色熒光)與蒽單元(發射藍色熒光)分別被引入到親水聚(N,N-二甲基丙烯酰胺)(PDMA)水凝膠網絡與疏水聚甲基丙烯酸十八烷基酯(PSMA)油凝膠網絡中。通過365nm紫外光的照射激發,蒽單元發生單體-二聚體轉變,完成其熒光顏色由藍色到無色的轉變。進一步疊加DEAN的黃綠色熒光,油水凝膠可以實現熒光顏色由藍色到淡黃色的轉變。借助光掩模可以實現精細圖案的存儲,并結合油凝膠分子網絡的結晶誘導形狀記憶特性,該多色油水凝膠可以實現熒光信息的加載存儲與加載信息隱藏在三維立體結構中的雙重加密-解密過程,從而使得信息具有更高的安全性。該工作近期以題為“Integrating photo-rewritable fluorescent information in shape-memory organohydrogel towards dual encryption”的論文發表在Adv. Opt. Mater.
3. 飛秒激光直寫3D仿生響應型水凝膠微致動器
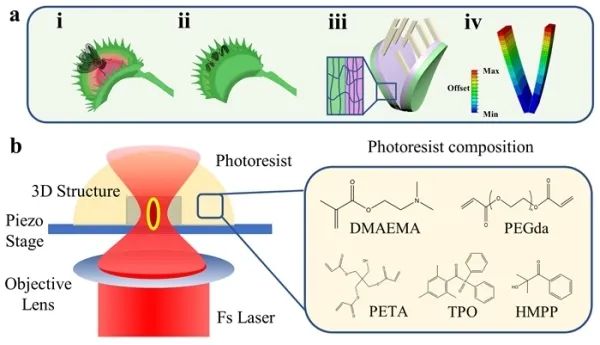
據中科院官網報道,中國科學院理化技術研究所仿生智能界面科學中心有機納米光子學實驗室研究員鄭美玲團隊在4D刺激響應型仿生水凝膠微致動器的制備及應用方面取得新進展。研究合成了刺激響應型光刻膠前驅體,并結合結構設計,采用飛秒激光直寫技術制備出4D刺激響應型水凝膠微結構。微米級水凝膠致動器表現出快速的pH響應,還可通過pH響應來調控微顆粒的捕獲和釋放行為。飛秒激光直寫技術是實現響應型水凝膠結構微型化的重要手段。該技術采用飛秒激光作為光源,激光束經物鏡聚焦到光刻膠中,基于非線性光學效應,聚合反應僅發生在光子數密度極高的中心區域,因此具有高精度、真三維的特點。研究利用刺激響應型光刻膠,優化飛秒激光直寫參數及激光加工路徑,獲得了響應行為可控的4D水凝膠微結構。研究改變激光加工參數來調節水凝膠微結構局部區域的交聯密度,從而獲得可控的pH響應行為,變形時間短至1.2秒,恢復時間為0.3秒。在此基礎上,科研人員受捕蠅草捕獲行為的啟發,設計并加工了仿生不對稱水凝膠微致動器,通過pH觸發,實現和調節了其形狀變化,捕獲了單個或多個微顆粒,并可控地實現了微顆粒的同時釋放或順次釋放。研究團隊對仿生水凝膠微致動器的控制操縱將增加精確捕獲和釋放微小物體的潛力,使智能水凝膠微致動器的制備成為可能。這種微致動器在軟體機器人、微傳感器和微電子機械系統(MEMS)等研究領域具有潛在的應用價值。
4.基于電滲膨壓的水凝膠基強快速致動器
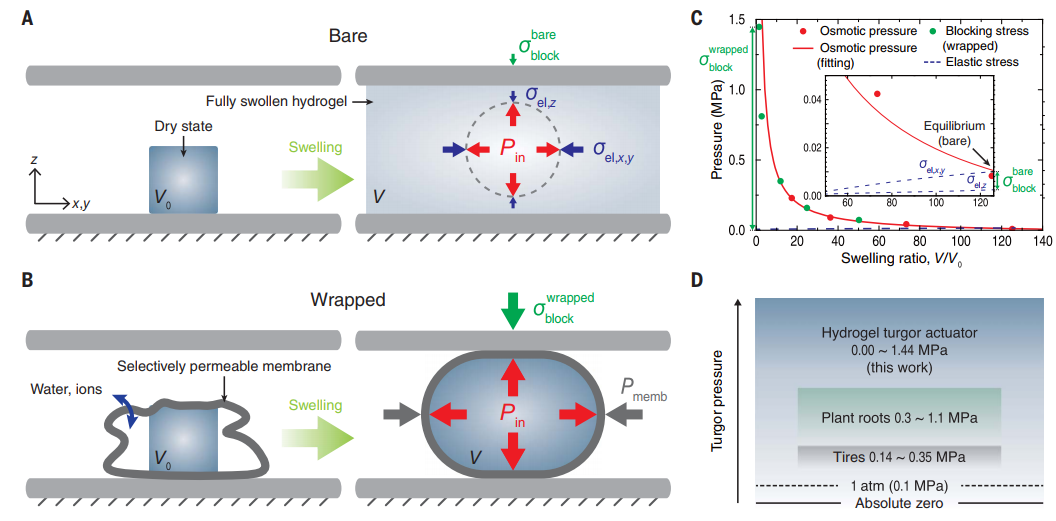
水凝膠,因其柔軟性、透明性和刺激響應性等優異性質,作為軟致動器材料,是極具前景的。然而,傳統刺激響應型水凝膠致動器,是采用滲透驅動的致動機制,致動力較弱,響應速度較慢。而且,能承受的壓力也很有限,如果壓力太大,傳統刺激響應型水凝膠致動器,就會崩潰或碎掉。主要是因為傳統刺激響應型水凝膠,低模量和滲透驅動的慢水擴散,使得弱和慢致動過程,仍然具有挑戰性。韓國 首爾大學Ho-Young Kim,Jeong-Yun Sun團隊Hyeonuk Na等,利用膨壓和電滲,實現水凝膠基強而快的致動器。選擇性滲透膜限制了凝膠制造的膨壓致動器,可以保持驅動凝膠膨脹的高滲透壓;因此,這種致動器用1.16立方厘米水凝膠制成,可以承受較大應力[在96分鐘(min)內0.73兆帕(MPa)]。電滲加速了水的傳輸,凝膠迅速溶脹,提高了啟動速度(9min內0.79MPa)。該實驗策略,使柔軟水凝膠,能夠在幾分鐘內打破壁壘brick,并快速構建水下結構。該項研究,將水凝膠包裹在相對堅硬但柔韌的半透膜中,顯著增加了水凝膠的驅動應力,這限制了橫向變形。這種效應類似于在生物細胞中看到的膨壓。向水溶液中加入電解質,并施加電場也可以提高驅動速度,從而將驅動時間從數小時縮短到數分鐘。該項研究以Hydrogel-based strong and fast actuators by electroosmotic turgor pressure為題,發表在Science上。
5. PVA/LiCl水凝膠電解質與MXene/CMC薄膜電極組裝超級電容器
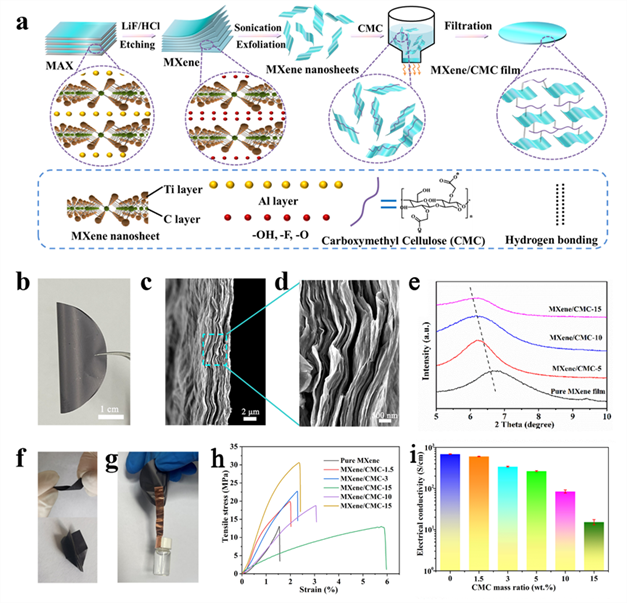
燕山大學焦體峰教授和秦志輝副教授課題組等人考慮到可穿戴超級電容器對高性能電極材料和水凝膠電解質的需求,首先通過對MXene和CMC分散體進行真空過濾及干燥制備了柔性MXene/羧甲基纖維素(CMC)薄膜電極。由于CMC與MXene納米片間的分子間相互作用,所得的MXene/CMC薄膜表現出高機械柔軟性(5.9%應變下的12.7MPa強度)和高電導率(267 S/cm)。對于水凝膠電解質的設計,通過利用LiCl調控PVA交聯網絡及水分子間的相互作用,制備了具有高拉伸性、自愈合性、高導電性、強黏附性及抗凍特性的PVA/LiCl水凝膠。最后,將PVA/LiCl水凝膠電解質與兩個MXene/CMC薄膜電極組裝成超級電容器。由于電解質和電極的高度機械柔軟性以及它們之間優異的界面相互作用,超級電容器可以在各種變形(如擠壓、扭曲和折疊)下保持出色的電化學穩定性。更重要的是,即使在-40°C下,這類超級電容器也能實現出色的機械柔韌性和高電容保持率。這些出色的性能使所設計的超級電容器有望成為可穿戴和便攜式電子設備的供能器件。該文章發表在Cell旗下期刊Cell Reports Physical Science上。尹娟娟為本文第一作者。
6. 體溫觸發快速粘附及按需剝離可逆粘附水凝膠助力無損傷皮膚護理

據中國海洋大學官網報道,中國海洋大學韓璐教授與西南交通大學魯雄教授合作,提出了一種基于多酚-蛋白質絡合策略制備具有體溫觸發快速粘附及無損傷按需剝離的水凝膠的策略。首先,通過堿性氧化預聚方式,形成了富含酚基和醌基的多酚預聚物(PGA);其次,在雙鍵化明膠(GelMA)成膠過程中利用多酚基團的多重相互作用,打破GelMA分子鏈間的氫鍵作用,調節GelMA鏈的纏結密度,使得GelMA網絡具有體溫響應性,實現在體溫條件下保持穩定性的同時分子鏈流動性增強的特性。當該水凝膠與人體皮膚接觸后,體溫觸發其發生相轉變實現高效快速粘附且能長時間保持粘附穩定。對水凝膠表面簡單的降溫后,網絡中的GelMA分子鏈間重新生成氫鍵,水凝膠粘附力降低,實現無損傷剝離。另外,PGA的引入調整了GelMA網絡的交聯方式,在GelMA網絡內引入了可犧牲的非共價鍵交聯,從而賦予PGA-GelMA水凝膠與皮膚組織匹配的機械柔韌性和高延展性,避免了水凝膠在皮膚表面剝離時被拉扯造成的傷害。此外,該PGA-GelMA水凝膠還表現出優異的抗炎、抗氧化、抗過敏等生物活性,能夠有效避免傳統皮膚粘合劑在長期與皮膚接觸中導致的皮膚刺激或過敏現象。相關研究以 “Infant skin friendly adhesive hydrogel patch activated at body temperature for bioelectronics securing and diabetic wound healing” 為題發表在《ACS Nano》。中國海洋大學的韓璐教授和西南交通大學魯雄教授為通訊作者,該工作得到了四川省重點研發計劃項目、國家自然科學基金等項目的支持
7. 多功能DNA水凝膠敷料促進糖尿病感染傷口愈合
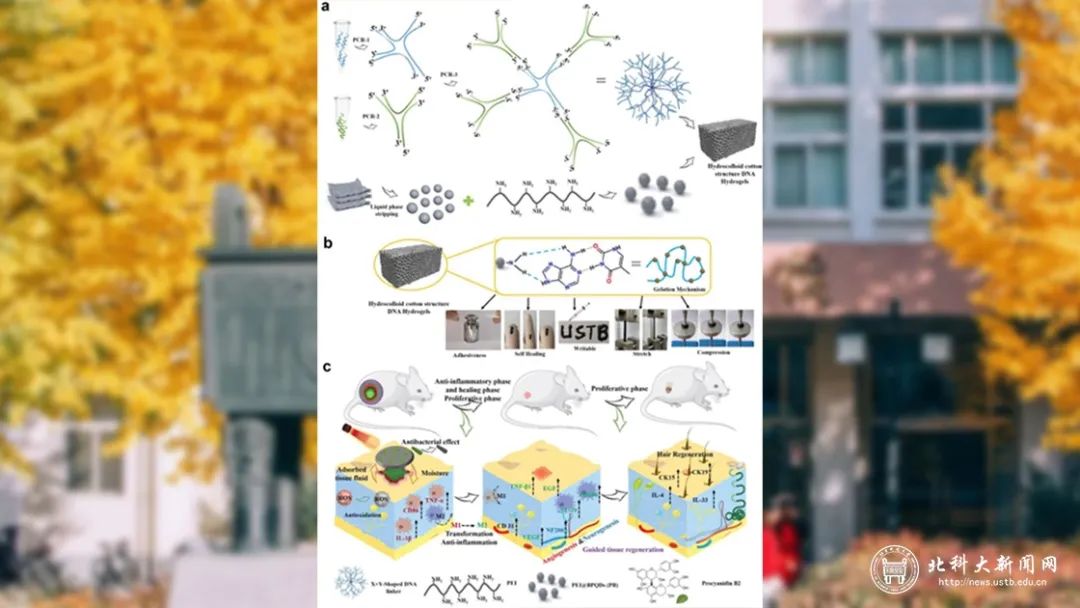
據中科大官網報道,化生學院化學系溫永強教授、生物系杜宏武教授等在“多功能DNA水凝膠敷料促進糖尿病感染傷口再生”方面的研究取得突破性進展,并在《Advanced Functional Materials》上發表研究性論文“Multifunctional DNA Hydrogels with Hydrocolloid-Cotton Structure for Regeneration of Diabetic Infectious Wounds”。作者設計了一種多功能的 DNA 水凝膠敷料。基于堿基配對原理,作者開發了樹枝狀大分子X+Y形DNA連接結構,然后與摻有黑磷量子點的聚乙烯亞胺動態交聯形成生物活性 DNA 水凝膠,并在其中加載OPC B2 作為一種天然營養素,具有抗氧化和清除自由基的能力,并能促進細胞增殖和血管生成。作者建立了全層皮膚感染的糖尿病小鼠模型,研究了體內糖尿病感染傷口的愈合性能。研究表明:水凝膠敷料提供的3D空間結構可以吸收大量膿液組織液,為傷口愈合提供了完美的環境。第6天,觀察到有新皮形成,而在第10天形成上皮層,可清晰觀察再生結構和新生毛囊組織。治療10天后,治療的傷口幾乎完全愈合,創面愈合率高達99.9%,而其他組的傷口沒有完全閉合。表明水凝膠在NIR觸發下具有優異的傷口愈合性能。
8. 通過水凝膠遞送miRNA抑制骨關節衰老促進軟骨再生新策略

浙江大學醫學院附屬邵逸夫醫院骨科方向前團隊和清華大學材料學院王秀梅團隊在《科學-進展》(Science Advances)上在線發表題為《基于干細胞歸巢水凝膠的miR-29b-5p遞送通過抑制衰老促進軟骨再生》(Stem cell-homing hydrogel-based miR-29b-5p delivery promotes cartilage regeneration by suppressing senescence in an osteoarthritis rat model)的研究成果,提出了通過抑制骨關節衰老促進軟骨再生治療OA的新策略,通過生物材料構建抑制衰老的再生微環境來使因OA受損的軟骨恢復活力。首次發現并驗證了OA軟骨衰老相關的miRNA(miR-29b-5p),并通過原位注射具有干細胞歸巢活性的自組裝多肽納米纖維水凝膠緩釋遞送miR-29b-5p,同時募集內源性滑膜間充質干細胞(SMSCs)。持續的miR-29b-5p遞送和干細胞的募集以及隨后分化成軟骨細胞實現了成功的軟骨修復和軟骨細胞再生。該研究表明基于miRNA的治療方式替代傳統手術治療OA具有巨大潛力。
9. 自修復、可回收和導電的水凝膠基應變傳感器
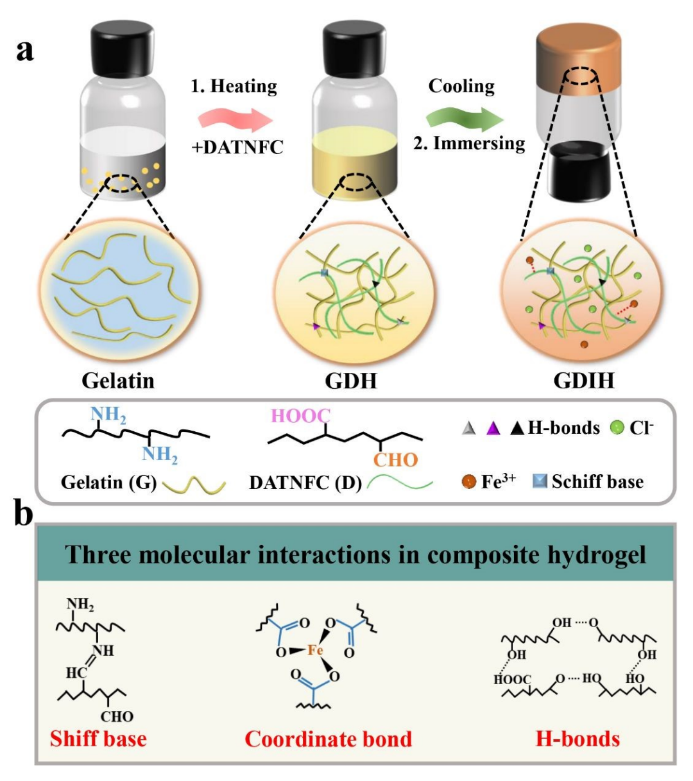
華南理工大學制漿造紙工程國家重點實驗室陳克復院士團隊報告了一種簡單的策略,通過分子水平的多重動態交聯作用(MMDI)設計了一種自修復、可回收和導電的水凝膠基應變傳感器,獲得的明膠/DATNFC/Fe3+水凝膠(GDIH)與純明膠水凝膠相比,拉伸強度和抗壓強度顯著增加,且有著優異的壓縮應力(1310 kPa)、自愈能力和導電性。該水凝膠被開發為多功能應變傳感器,具有高應變靈敏度和壓縮靈敏度,可用于制造電子皮膚并準確識別檢測微小變形引起的電生理信號,具有傳感穩定性和快速壓縮響應時間(200 ms)。MMDI水凝膠是通過溶膠-凝膠反應和離子浸入法制備的,無需復雜的分子設計和化學反應,主要由明膠、改性修飾納米纖維素(DATNFC)和Fe3+組成多重動態交聯網絡,能夠可逆地斷裂和重建,提供了凝膠優異的機械性能和優異的自愈能力。與純明膠相比,拉伸強度和壓縮強度分別提高了990.7%和3822.7%。上述研究以“A Self-healing, Recyclable and Conductive Gelatin/Nanofibrillated Cellulose/Fe3+ Hydrogels Based on Multi-Dynamic Interactions for Multifunctional Strain Sensors”為題發表在《Materials Horizons》上
免責聲明:本網站所轉載的文字、圖片與視頻資料版權歸原創作者所有,如果涉及侵權,請第一時間聯系本網刪除。

官方微信
《腐蝕與防護網電子期刊》征訂啟事
- 投稿聯系:編輯部
- 電話:010-62316606-806
- 郵箱:fsfhzy666@163.com
- 腐蝕與防護網官方QQ群:140808414





