引言
水凝膠是一種網(wǎng)狀結(jié)構(gòu)的親水性聚合物材料。親水性聚合物鏈通過交聯(lián)而形成三維固體,水則充當(dāng)分散介質(zhì)。水凝膠材料具有極高的吸水性,其材料質(zhì)地通常很軟且不夠強(qiáng)壯。但是通過定向設(shè)計(jì),水凝膠材料可以變的很有韌性。除此之外,水凝膠材料具有極好的生物兼容性和離子傳送能力,從而使之有被廣泛運(yùn)用于仿生材料和人造組織等醫(yī)學(xué)領(lǐng)域的潛力。在這篇文章中,我們通過回顧近期發(fā)表在Nature及其子刊上的研究成果,總結(jié)了水凝膠材料最新研究成就和當(dāng)前研究方向,為正在此研究方向或有志從事此研究方向的學(xué)者們提供參考。
01 具有抗菌和血管生成特性的可注射自我修復(fù)水凝膠
該功能性水凝膠旨在應(yīng)對糖尿病患者的傷口再生問題。臨床研究表明,糖尿病可導(dǎo)致肌腱,骨骼和關(guān)節(jié)慢性潰爛且無法治愈。迄今為止,糖尿病引起的患者下肢截肢案例已超過2000萬起,于此同時(shí),每年需要截肢的患者數(shù)量將翻一番。而這一系列糖尿病并發(fā)癥的原因在于血管形成受損,尤其是微脈管形成受損,這對于氧氣輸送和傷口愈合至關(guān)重要。缺少足夠的毛細(xì)血管,患者傷口部位會積累大量的葡萄糖,從而導(dǎo)致組織壞死。因此,在愈合早期,重建毛細(xì)血管網(wǎng)絡(luò)對于防止患者傷口擴(kuò)張和潰爛的形成有著至關(guān)重要的意義。上海交通大學(xué)醫(yī)學(xué)院附屬瑞金醫(yī)院鄧廉夫團(tuán)隊(duì)研究設(shè)計(jì)了一種具有抗菌和血管生成特性的可注射,自我修復(fù)的協(xié)調(diào)性水凝膠材料。該材料可用于糖尿病傷口的再生。實(shí)驗(yàn)團(tuán)隊(duì)通過多臂硫醇化聚乙二醇(SH-PEG)與硝酸銀的配位交聯(lián)制備水凝膠。由于Ag-S配位鍵的動態(tài)性質(zhì)和Ag離子的殺菌作用,所得的配位水凝膠材料具有自我修復(fù),可注射和抗菌特性。除此之外,實(shí)驗(yàn)團(tuán)隊(duì)還在水凝膠材料中加載了血管生成藥物去鐵胺(DFO),得到了一種多功能,易處理,抗菌且具有血管生成能力的水凝膠材料。實(shí)驗(yàn)結(jié)果顯示,添加藥物的功能性水凝膠可以通過0.5 mm針頭完成注射,具有有效的抗菌能力且擁有較好的生物相容性。在體外實(shí)驗(yàn)中,材料展現(xiàn)出了優(yōu)秀的靈活性,抗菌能力和對外界物理刺激的阻止能力;在動物實(shí)驗(yàn)中,團(tuán)隊(duì)驗(yàn)證了該材料對血管再生的促進(jìn)作用和抗菌能力。這一成果不僅為糖尿病引發(fā)的傷口愈合問題提供了解決辦法,也為其他類型的傷口愈合,尤其是暴露于細(xì)菌環(huán)境下的傷口,提供了解決思路。
圖1
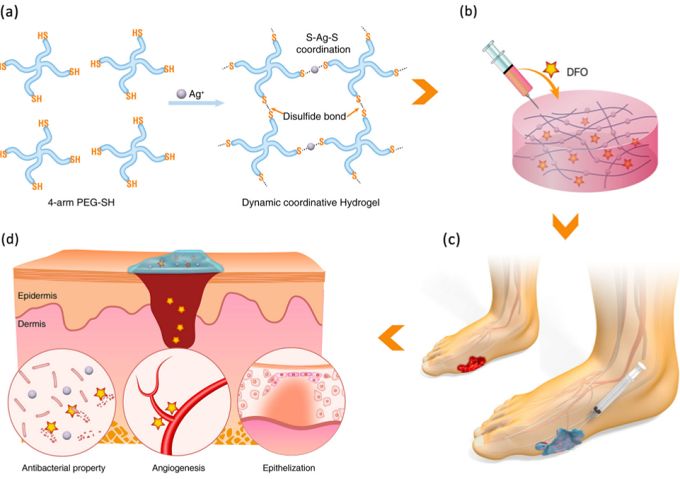
a) 自愈性含銀硫醇配位水凝膠合成示意圖;
b) 注入血管生成藥物獲得可自我修復(fù),可注射,抗菌,多功能水凝膠;
c) I型糖尿病足潰瘍(左)和水凝膠治療后效果(右);
d) 水凝膠修復(fù)作用機(jī)制示意圖。[1]
02 具有強(qiáng)粘性的止血水凝膠
不可控出血是重大創(chuàng)傷和外科手術(shù)過程中經(jīng)常遇到的問題。不可控出血是目前全球死亡率高的一個(gè)主要原因。其中,修復(fù)主動脈破裂和心臟穿透傷口引起的心臟出血是外科手術(shù)的難點(diǎn)。目前常用的止血劑對于濕環(huán)境和運(yùn)動組織的粘附力較弱,很難控制創(chuàng)傷性動脈和心臟傷口的出血。外科手術(shù)縫合是當(dāng)前唯一用于主動脈破裂和心臟傷口密封的臨床方法。然而,這在大多數(shù)醫(yī)院環(huán)境外和緊急情況下都不可行。隨著材料科技的發(fā)展,科學(xué)家們研究出了許多快速傷口密封材料,如纖維蛋白膠,明膠,氧化纖維素,肽等。然而,由于這些材料在濕組織表面粘附性差,粘結(jié)機(jī)制較弱,這些材料并不適用于主動脈和心臟外傷止血。用于動脈及心臟組織處的快速密封性材料需要在連續(xù)流動的情況下快速粘合,在濕組織壁和表面之間具有強(qiáng)粘合力,擁有可以承受血壓的高機(jī)械強(qiáng)度以及生物相容性。最近,浙江大學(xué)醫(yī)學(xué)院二附院歐陽宏偉教授和他的團(tuán)隊(duì)設(shè)計(jì)了一種仿生組織水凝膠粘合劑材料。這種材料可以在幾秒內(nèi)聚合并粘附。在紫外線光激活后牢固地粘合到濕生物組織表面。該材料的設(shè)計(jì)受到生物結(jié)締組織的細(xì)胞外基質(zhì)的啟發(fā)。實(shí)驗(yàn)小組設(shè)計(jì)的水凝膠生物粘合劑由5%的甲基丙烯酸明膠(GelMA),1.25%的N-(2aminoethyl)?4-(4-(hydroxymethyl)?2-methoxy-5-nitrosophenoxy) butanamide (NB)連接糖胺聚糖透明質(zhì)酸(HA-NB)和0.1%的聚合引發(fā)劑苯基-2,4,6-三甲基苯甲酰基次膦酸鋰(LAP)。將甲基丙烯酸明膠(GelMA)引入水凝膠可保持其濕傷口密封的能力,并大幅度加速聚合,避免了未聚合的材料在形成鍵合凝膠之前被血流沖走,從而大大提高了這種傷口密封水凝膠的臨床實(shí)用性。實(shí)驗(yàn)結(jié)果顯示,由該材料修復(fù)的血管可以承受高達(dá)290 mmHg的血壓,高于大多數(shù)臨床情況下的血壓(收縮壓BP 60-160 mmHg)。除此之外,動物實(shí)驗(yàn)顯示,該水凝膠可以20s內(nèi)阻止4~5 mm長切口傷口的豬頸動脈和直徑為6 mm的心臟穿透孔的豬心臟高壓出血且不使用縫合線。用該水凝膠進(jìn)行止血治療后的豬成功存活了下來。這種不需要縫合即可實(shí)現(xiàn)快速止血和密封的材料,有望被運(yùn)用于外科手術(shù)和緊急止血。
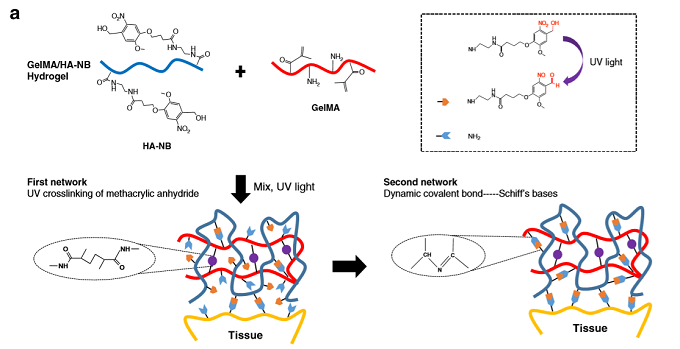
圖2 材料成分和結(jié)構(gòu)示意圖及光誘導(dǎo)合成材料流程示意圖。
03 具有各向異性響應(yīng)驅(qū)動能力的自修復(fù)水凝膠
許多活體生物體內(nèi),大多數(shù)組織具有從分子水平到宏觀水平的各向異性形態(tài),結(jié)構(gòu)和反應(yīng)。例如,緊密平行排布結(jié)構(gòu)的膠原纖維使肌肉具有顯著的一維方向上的收縮力。由于具有良好的生物相容性和生物系統(tǒng)的相似性,水凝膠被廣泛用作人造器官或者組織工程的聚合物支架。然而,大多數(shù)水凝膠通常表現(xiàn)出各向同性結(jié)構(gòu),從而導(dǎo)致在接受外界刺激時(shí)發(fā)生非定向形變。受到智能生物組織的啟發(fā),中國科技大學(xué)從懷萍教授和她的團(tuán)隊(duì)設(shè)計(jì)了一種由高度有序的層狀網(wǎng)絡(luò)結(jié)構(gòu)組成的,以金屬鈉米結(jié)構(gòu)為裝配結(jié)構(gòu)的各向異性水凝膠材料(材料結(jié)構(gòu)可見于圖3)。實(shí)驗(yàn)團(tuán)隊(duì)提出使用金納米顆粒的動態(tài)硫醇鹽(RS-Au)配位作為水凝膠的交聯(lián)連接方式。這種方式可以實(shí)現(xiàn)當(dāng)材料內(nèi)部發(fā)生較大形變時(shí),引起的缺口區(qū)域得以自我修復(fù)。由于動態(tài)RS-Ag相互作用的存在,該水凝膠材料顯示出由NIR激光和酸性條件誘導(dǎo)的快速有效的多響應(yīng)自我修復(fù)功能。有趣的是,一些復(fù)雜的驅(qū)動行為,例如使用機(jī)械臂抬起和抓取動作,可以通過誘導(dǎo)愈合具有不同結(jié)構(gòu)的水凝膠碎片來實(shí)現(xiàn)(驅(qū)動過程可見圖4),從而實(shí)現(xiàn)具有運(yùn)用價(jià)值的軟體驅(qū)動器。實(shí)驗(yàn)結(jié)果顯示,該材料在機(jī)械,光學(xué),膨脹和消脹行為上的各向異性。其平行方向模量是垂直方向模量的3.9倍。該各向異性水凝膠材料在未來研究和開發(fā)智能機(jī)器人等高級軟體驅(qū)動器有著巨大的潛力。
圖3 合成SNPP水凝膠材料的圖像示意圖。
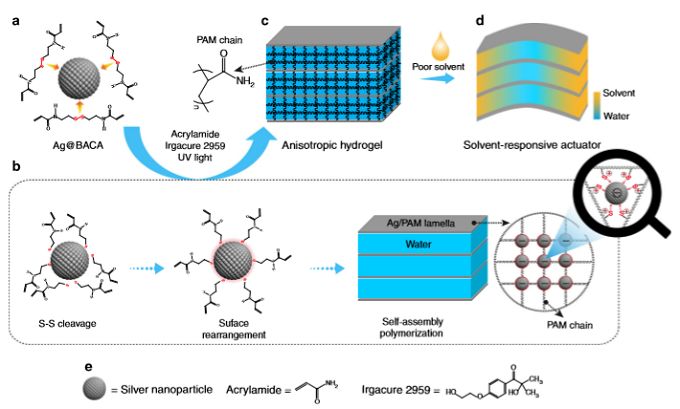
a. Ag@BACA 微粒與RS-Ag配位鍵相連;
b. 當(dāng)BACA分子吸附到微粒上后,S-S鍵斷開,在紫外線光的照射下,BACA分子重新排布,并在聚合反應(yīng)和疏水作用下于水凝膠上生成Ag/PAM層;
c. 通過PAM材料鏈?zhǔn)浇Y(jié)構(gòu)的生長和紫外線光的照射作用,各向異性的水凝膠被準(zhǔn)備完成;
d. 所制得材料在收到外界溶劑環(huán)境變化時(shí)引起的定向形變行為。[3]
圖4 該水凝膠成果在軟體驅(qū)動器上運(yùn)用原理示意圖。
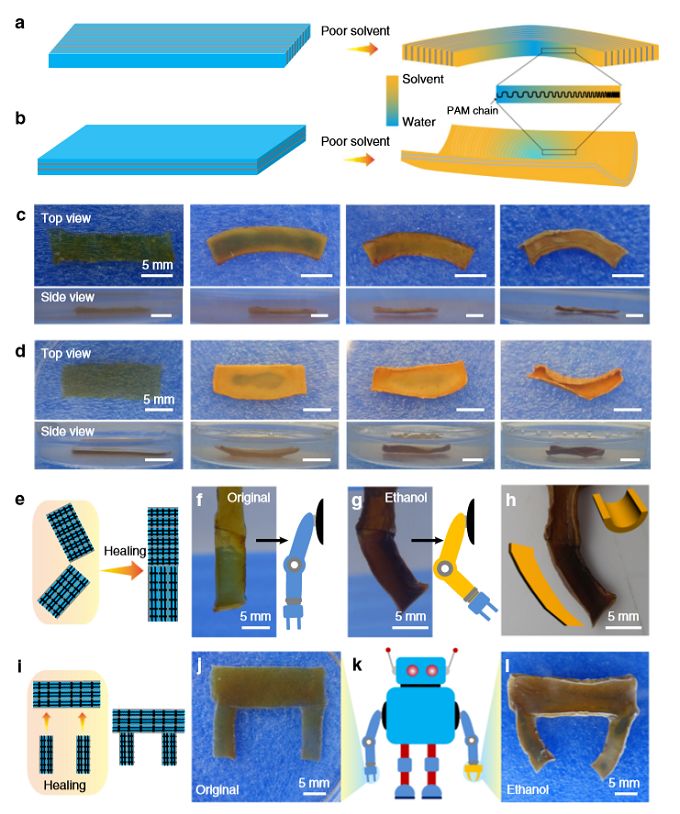
實(shí)驗(yàn)團(tuán)隊(duì)設(shè)計(jì)的水凝膠在受到外界溶劑環(huán)境刺激時(shí)會向垂直于層狀結(jié)構(gòu)的方向彎曲(a - d)。實(shí)現(xiàn)團(tuán)隊(duì)利用這一特性,將材料碎片按照不同結(jié)構(gòu)方向整合安裝(e和i),使集成結(jié)構(gòu)有定向彎曲形變的能力,從而實(shí)現(xiàn)軟體機(jī)械臂的抓取行為。[3]
04 可用于骨組織工程的多孔水凝膠
目前,盡管科學(xué)家們已經(jīng)探索出了利用組織工程學(xué)生產(chǎn)天然材料和合成材料。但是純化天然材料的復(fù)雜性,機(jī)械特性和免疫原性嚴(yán)重限制了這類材料的運(yùn)用。這一列原因使得引導(dǎo)干細(xì)胞促進(jìn)骨組織再生頗具挑戰(zhàn)。受到醫(yī)療器械領(lǐng)域生物材料的發(fā)展,科學(xué)家們注意到了粘土和粘土礦物作為新興生物材料用于骨組織再生的潛力。蒙脫土(MMT)是膨潤土的主要組成部分。近年來,這種特殊粘土礦物的生物相容性,可用性和可行性引起了很大的關(guān)注。一些報(bào)告指出,可以通過天然生物材料(如明膠,膠原蛋白,蠶絲)中引入MMT來制造支架,改善細(xì)胞支架的相互作用,增殖和分化。但盡管這些材料具有多孔結(jié)構(gòu),但其制備生產(chǎn)過程(真空,低溫)無法適用于組織工程學(xué)中。
美國加州洛杉磯大學(xué)的Min Lee教授和他的團(tuán)隊(duì)注意到源自天然產(chǎn)物的水凝膠材料為解決骨組織成長提供了一種潛在可行的解決方法。與需要預(yù)先在嚴(yán)苛環(huán)境下成型的硬質(zhì)支架相比,軟質(zhì)水凝膠是可注射的,而且可以以最小的方式填充任何不規(guī)則形狀的缺陷。在研究中,他們通過引入具有插層化學(xué)作用的二維納米粘土顆粒,成功地納米工程化了互連的微孔網(wǎng)絡(luò)化可光交聯(lián)的殼聚糖在原位形成水凝膠。納米硅酸鹽的存在增加了楊氏模量并阻止了所得水凝膠的降解速率。實(shí)驗(yàn)結(jié)果證明增強(qiáng)的水凝膠促進(jìn)了增殖作用,并誘導(dǎo)體外封裝的間充質(zhì)干細(xì)胞的分化。在小鼠活體實(shí)驗(yàn)中,實(shí)驗(yàn)小隊(duì)用臨界大小的小鼠顱蓋缺損模型探究了納米工程水凝膠在體內(nèi)的作用。實(shí)驗(yàn)結(jié)果證實(shí),殼聚糖-蒙脫石水凝膠能夠附著天然細(xì)胞并促進(jìn)顱蓋愈合。這一實(shí)驗(yàn)成果證明了該材料在組織工程學(xué)領(lǐng)域的運(yùn)用潛力。
圖5 內(nèi)部連接的微孔狀結(jié)構(gòu)SEM圖像。圖像對應(yīng)不同比重MMT材料下的微觀結(jié)構(gòu)圖。[4]

05 可適用于大腦表面的水凝膠有機(jī)硬膜下電極
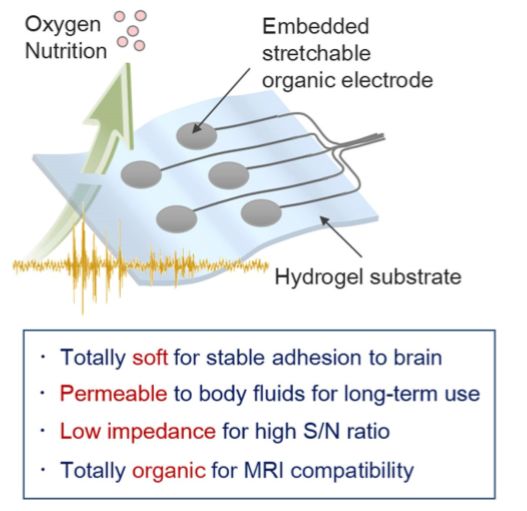
神經(jīng)生理學(xué)檢測已廣泛用于診斷和治療神經(jīng)系統(tǒng)疾病,例如癲癇和慢性疼痛。在需要手術(shù)切除癲癇或腦腫瘤的神經(jīng)外科手術(shù)之前和期間,通過監(jiān)視或映射腦功能來識別病理性病變非常重要。皮層腦電圖(ECoG)或顱內(nèi)腦電圖(iEEG)是一種通過硬膜下電極進(jìn)行的神經(jīng)生理學(xué)檢測。硬腦膜下電極位于大腦皮層表面,因此在空間分辨率和信號質(zhì)量上優(yōu)于頭皮腦電圖(EEG)。此時(shí),高信噪比和低偽影在監(jiān)視或映射大腦功能中尤為重要。因此,硬膜下電極比頭皮電極在手術(shù)前的監(jiān)測中更有用,也更有望最大程度保護(hù)腦功能。盡管ECoG優(yōu)于EEG,但是由于ECoG-fMRI中使用的金屬電極會感應(yīng)射頻,因此到目前為止,它尚未被廣泛運(yùn)用于臨床領(lǐng)域。另外,MRI引起的顱內(nèi)金屬電極的感應(yīng)加熱是帕金森病長期深層腦刺激(DBS)的缺點(diǎn)。除了加熱問題以外,電極與皮質(zhì)之間的接觸也是一個(gè)具有挑戰(zhàn)性的問題。皮質(zhì)與由金屬制成的常規(guī)ECoG電極之間的松動接觸會導(dǎo)致信號不準(zhǔn)確和潛在的誤診。雖然已經(jīng)有團(tuán)隊(duì)研究出基于塑料薄膜的超薄電極用于改進(jìn)接觸問題,但是塑料薄膜存在操作難度大和無法滲透體液進(jìn)而導(dǎo)致阻礙了組織液循環(huán)的缺點(diǎn)。最近,日本東北大學(xué)的Matsuhiko nishizawa教授和他的團(tuán)隊(duì)開發(fā)了一種有機(jī)ECoG電極材料。該電極由水凝膠基質(zhì)和帶圖案的可拉伸碳纖維材料組成(CF)。與金屬電極相比,該材料具有較低的磁化率和電阻率,因此它降低了MRI期間產(chǎn)生圖像偽影和發(fā)熱的風(fēng)險(xiǎn)。通過PEDOT進(jìn)行了改進(jìn)后,材料在工作頻率上具有了更好的阻抗特性。該團(tuán)隊(duì)設(shè)計(jì)開發(fā)的水凝膠為基礎(chǔ)的新材料具有幾大優(yōu)勢:與活組織擁有相似的機(jī)械性能,易于操作,對大腦表面的粘附性更好以及對體液具有滲透性。PEDOT-CF/hydrogel硬膜下電極能夠以高空間分辨率監(jiān)控ECoG,為獲取清晰的MRI圖像和準(zhǔn)確的信號提供了一種解決方案。
圖6 有機(jī)水凝膠硬膜下電極設(shè)計(jì)示意圖及其優(yōu)點(diǎn)。 [5]
參考文獻(xiàn)
Chen, H., Cheng, R., Zhao, X., Zhang, Y., Tam, A., & Yan, Y. et al. (2019)。 An injectable self-healing coordinative hydrogel with antibacterial and angiogenic properties for diabetic skin wound repair. NPG Asia Materials, 11(1)。 doi: 10.1038/s41427-018-0103-9
Hong, Y., Zhou, F., Hua, Y., Zhang, X., Ni, C., & Pan, D. et al. (2019)。 A strongly adhesive hemostatic hydrogel for the repair of arterial and heart bleeds. Nature Communications, 10(1)。 doi: 10.1038/s41467-019-10004-7
Qin, H., Zhang, T., Li, N., Cong, H., & Yu, S. (2019)。 Anisotropic and self-healing hydrogels with multi-responsive actuating capability. Nature Communications, 10(1)。 doi: 10.1038/s41467-019-10243-8
Cui, Z., Kim, S., Baljon, J., Wu, B., Aghaloo, T., & Lee, M. (2019)。 Microporous methacrylated glycol chitosan-montmorillonite nanocomposite hydrogel for bone tissue engineering. Nature Communications, 10(1)。 doi: 10.1038/s41467-019-11511-3
Oribe, S., Yoshida, S., Kusama, S., Osawa, S., Nakagawa, A., & Iwasaki, M. et al. (2019)。 Hydrogel-Based Organic Subdural Electrode with High Conformability to Brain Surface. Scientific Reports, 9(1)。 doi: 10.1038/s41598-019-49772-z
免責(zé)聲明:本網(wǎng)站所轉(zhuǎn)載的文字、圖片與視頻資料版權(quán)歸原創(chuàng)作者所有,如果涉及侵權(quán),請第一時(shí)間聯(lián)系本網(wǎng)刪除。

官方微信
《中國腐蝕與防護(hù)網(wǎng)電子期刊》征訂啟事
- 投稿聯(lián)系:編輯部
- 電話:010-62313558-806
- 郵箱:fsfhzy666@163.com
- 中國腐蝕與防護(hù)網(wǎng)官方QQ群:140808414





