核能是一種清潔能源,核能發(fā)電排放的溫室氣體量僅為傳統(tǒng)化石燃料的1/50[1]。近幾十年來我國核能行業(yè)迅速發(fā)展,核電廠在滿足全國供電需求的同時,也將產(chǎn)生大量的核廢料,據(jù)估算,截止到2020年,這些核廢料總量約83000 t HM[2],因此,需要將這些核廢料妥善處置。其中,高放射性廢物(HLW)由于放射性水平高、半衰期長、熱量大、毒性大等[3~5]特點需要進行永久處置以避免危害人類生活。目前各國認可的處置高放廢物的方式為深地質(zhì)處置。2006年,我國發(fā)布了首個高放廢物地質(zhì)處置的政府文件《高放廢物地質(zhì)處置研究開發(fā)規(guī)劃指南》,并計劃在2050年建成中國高放廢物處置庫(DGR)[6]。經(jīng)過多年考察,我國已經(jīng)選擇甘肅北山地區(qū)為建造深地質(zhì)處置庫的預選場址[7]。
在DGR中會經(jīng)歷從初期的有氧、高溫環(huán)境到后期氧含量降低至接近為零,溫度逐漸下降20℃左右的漫長演變過程[4],核廢料的放射性降低到原來鈾礦的放射水平也需要近萬年時間[8~10]。因此金屬儲罐作為使核廢料與外界環(huán)境完全隔離的屏障之一,其設計使用壽命需要達到萬年以上[11]。在金屬儲罐的候選材料中,Cu和碳鋼被研究的最多。碳鋼因其硬度大、塑性好、腐蝕行為可預測、價格低廉等優(yōu)點被許多國家選為候選材料,如法國、瑞士、日本和比利時等國家;Cu因為有良好的耐蝕性,且相比其他耐蝕性金屬,Cu在含有Cl-的溶液中通常發(fā)生均勻腐蝕,被加拿大、芬蘭、瑞典等國家選用候選材料[12]。目前,我國暫未確定金屬儲罐的制作材料,近幾年對低碳鋼在深地質(zhì)環(huán)境中的腐蝕行為研究較多[13~16],但碳鋼的缺點是耐蝕性較差。加拿大曾提出在碳鋼表面鍍一層銅鍍層以提高金屬儲罐的耐蝕性[17],鍍銅鋼儲罐結合了碳鋼和銅的優(yōu)點,可以作為金屬儲罐的候選材料之一。但是當銅鍍層表面出現(xiàn)缺陷時,內(nèi)部碳鋼暴露,銅和碳鋼在地下水溶液中存在發(fā)生電偶腐蝕的風險,加快金屬儲罐的腐蝕失效速度。因此,若選擇鍍銅鋼作為我國金屬儲罐材料,需充分考慮銅和碳鋼在北山地下水環(huán)境中的電偶腐蝕。
我國北山地區(qū)地下水中主要的侵蝕性離子為
1 實驗方法
實驗所用金屬材料為T2銅合金和Q235鋼,均購自山東晟鑫科技有限公司。T2銅合金的化學成分(質(zhì)量分數(shù),%)為:Zn 0.005,Pb 0.005,Sn 0.002,Ni 0.005,F(xiàn)e 0.005,Sb 0.002,S 0.005,As 0.002和Cu余量,Q235鋼的化學成分(質(zhì)量分數(shù),%)為:C 0.181,Si 0.208,P 0.041,S 0.035,Al 0.266,Mn 0.552,Cu 0.167和Fe余量。采用線切割的方式將兩種金屬材料加工成高度為5 mm,直徑不同的圓柱形金屬試樣,其中T2銅合金的直徑分別為25.3和56.6 mm,Q235鋼的直徑為4和8 mm,通過組合不同面積的銅合金和碳鋼,形成不同面積比的電偶對。選擇試樣的任一圓形面為工作面,相對的另一面焊接銅導線后,用環(huán)氧樹脂密封,制成電極。工作面分別用400#,600#,800#,1000#,1500#以及3000#的SiC砂紙逐級濕磨,打磨好后用無水乙醇超聲清洗10 min后用N2吹干,放入玻璃干燥器中備用。實驗中所有溶液均采用分析純試劑和電阻率為18.2 MΩ·cm的超純水配制。北山地下水中主要陽離子為Ca2+、Na+、K+和Mg2+,陰離子為Cl-、
使用CHI 604E電化學工作站分別測試T2銅合金和Q235鋼的開路電位(OCP),在三電極體系,其中參比電極為飽和Ag/AgCl電極(0.198 V vs. SHE),對電極為1 cm × 1 cm的Pt電極,測試時間持續(xù)1 h。極化曲線和電偶腐蝕實驗使用內(nèi)置有零電阻電流計(ZRA)的Ivium-n-Stat多通道電化學工作站進行測試。進行極化曲線測試時掃描速率為10 mV·min-1,掃描范圍為OCP ± 300 mV。電偶腐蝕實驗中,Q235鋼為工作電極,T2銅合金為對電極,參比電極為飽和Ag/AgCl電極,實驗中始終保持工作電極和對電極的距離約為1 cm。組裝好的電解池固定好后放入恒溫箱中保持溫度為25或50℃,實驗開始前,用氣泵向溶液中通空氣3 h以保持有氧狀態(tài),并持續(xù)通氣至測試結束,待電偶電流和電偶電壓穩(wěn)定后,記錄最后10 h數(shù)據(jù)取平均值。實驗結束后,將需要進行表面分析的Q235鋼電極小心取出,用超純水清洗表面(不破壞腐蝕產(chǎn)物),無水乙醇脫水、N2吹干后暫放于手套箱中。
使用Regulus 8100場發(fā)射掃描電子顯微鏡(SEM)對Q235鋼表面進行腐蝕產(chǎn)物形貌表征,LabRAM HR Evolution拉曼光譜儀(Raman,激發(fā)波長633 nm,掃描范圍為100~2000 cm-1)進行腐蝕產(chǎn)物組成分析,DDS-11A電導率儀對溶液的電導率進行測試。
2 結果與討論
2.1 OCP測試
圖1
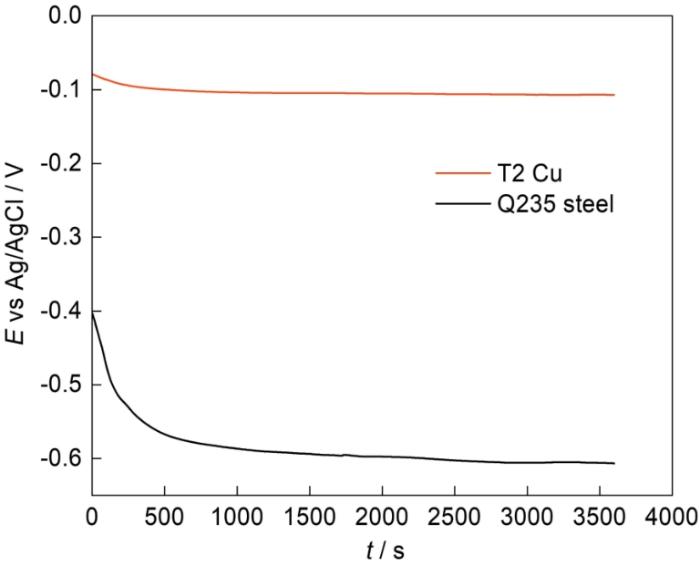
圖1 T2銅合金和Q235鋼在北山地下水模擬液中的OCP-t曲線
Fig.1 OCP-t curves of T2 Cu-based alloy and Q235 steel in simplified Beishan groundwater simulation fluid
25℃時Cl-濃度變化對T2銅合金和Q235鋼OCP的影響如圖2所示。Cl-濃度從0.001 mol·L-1增大到2 mol·L-1,T2銅合金的OCP整體出現(xiàn)明顯的負移,負移值為230 mV;Q235鋼的OCP先負移,后在0.05 mol·L-1到0.1 mol·L-1之間出現(xiàn)波動,最后在2 mol·L-1時又正移到-0.56 V,與在0.001 mol·L-1時數(shù)值幾乎相同。可以看出,隨著Cl-濃度增大,在一定濃度范圍內(nèi),T2銅合金和Q235鋼的OCP均出現(xiàn)了明顯的負移,表明Cl-濃度從0.001 mol L-1增大到0.05 mol·L-1時,銅合金和碳鋼的腐蝕傾向均增加。當Cl-濃度繼續(xù)增大時,T2銅合金的OCP在0.05 mol·L-1后出現(xiàn)小幅正移后又繼續(xù)大幅負移,表明T2銅合金在Cl-濃度較大時腐蝕傾向也在增加;而Q235鋼的OCP在0.1 mol·L-1到1 mol·L-1出現(xiàn)小幅度負移,在1 mol·L-1之后出現(xiàn)明顯的正移,表明Q235鋼的腐蝕傾向在1 mol·L-1之后減小。T2銅合金和Q235鋼OCP之間的差值在Cl-濃度大于0.1 mol·L-1時逐漸減小,表明它們之間的耦合效應可能在Cl-濃度較大時逐漸減弱。
圖2
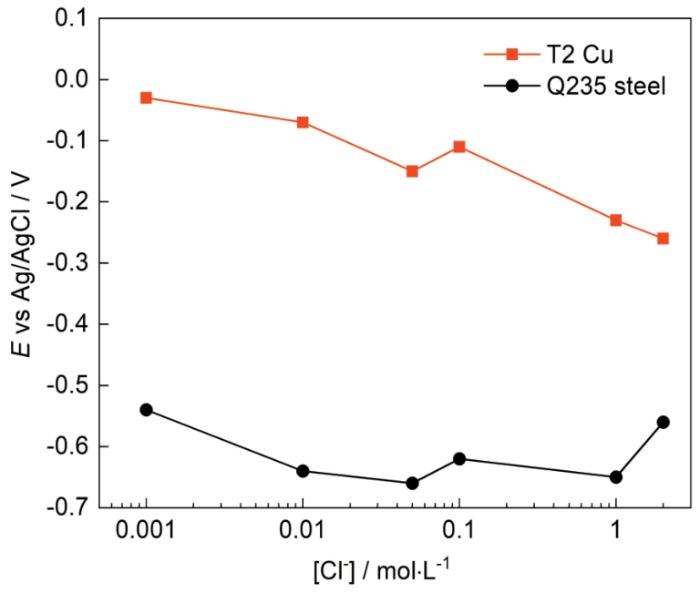
圖2 25℃時Cl-濃度對T2銅合金和Q235鋼OCP的影響
Fig.2 Influences of Cl- concentration on OCP values of T2 Cu-based alloy and Q235 steel at 25oC
2.2 極化曲線測試
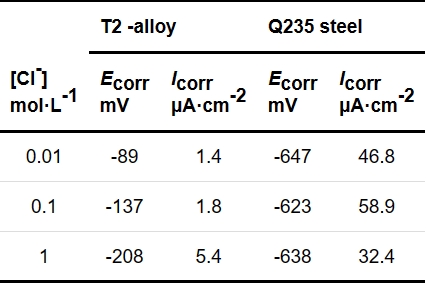
為進一步探究Cl-濃度變化對T2銅合金和Q235鋼腐蝕行為的影響,分別在0.01、0.1、1 mol·L-1溶液中對T2銅合金和Q235鋼進行極化曲線測試,測試結果如圖3所示,表1為極化曲線擬合結果。如圖3a所示,T2銅合金的陰極極化受氧擴散控制,陽極極化表現(xiàn)為金屬的活性溶解;在Cl-濃度為0.01和1 mol·L-1時,T2銅合金的陽極極化分支出現(xiàn)鈍化現(xiàn)象,是由于在Cl-濃度較大時,銅合金表面形成了比較致密的鈍化膜,使得電流密度出現(xiàn)了短暫的下降;隨后鈍化膜被擊穿,電流密度繼續(xù)升高。T2銅合金的腐蝕電位Ecorr隨Cl-濃度增大出現(xiàn)負移,與OCP的結果相對應;腐蝕電流密度Icorr隨Cl-濃度增大而增大,表明Cl-濃度增大會使T2銅合金的腐蝕速率加快。在圖3b中,Q235鋼的陰極極化明顯也受氧擴散控制,陽極極化均表現(xiàn)為金屬的活性溶解,沒有出現(xiàn)鈍化現(xiàn)象。Ecorr先正移后有所負移,Icorr先增大后減小,表明隨Cl-濃度增大,Q235鋼的腐蝕速率先增大后減小,過高的Cl-濃度會抑制Q235鋼的腐蝕。從表1數(shù)據(jù)可以看出,在相同的溶液中,T2銅合金的腐蝕速率會明顯低于Q235鋼。因此對于“鍍銅鋼”金屬儲罐,在銅鍍層未發(fā)生破損前,具有比碳鋼更好的耐蝕性,可以有效延長金屬儲罐的使用壽命。
圖3
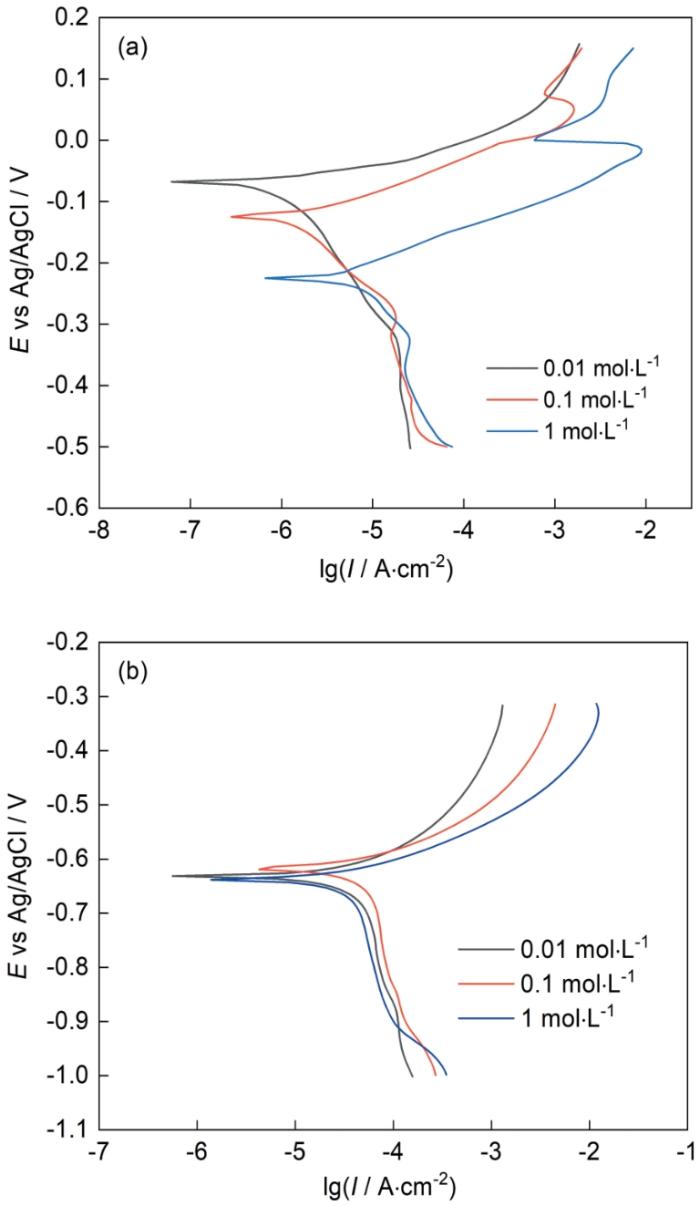
圖3 T2銅合金和Q235鋼在25℃含不同Cl-濃度的溶液中的極化曲線
Fig.3 Polarization curves of T2 Cu-based alloy (a) and Q235 steel (b) in test solutions with different Cl- concentrations at 25oC
表1 T2銅合金和Q235鋼的極化曲線擬合參數(shù)
Table 1
2.3 電偶腐蝕實驗
一旦銅鍍層發(fā)生破損并裸漏出碳鋼基體,可能會導致碳鋼基體發(fā)生嚴重的腐蝕。在鍍銅鋼材料中,銅鍍層直接與鋼基體接觸,無法直接測試電偶電壓和電偶電流[20],且在實驗中如果銅鍍層出現(xiàn)進一步破損,則電偶對的面積比將發(fā)生變化,影響實驗結果的準確性。因此,本研究中將金屬材料T2銅合金和Q235鋼分別做成電極進行實驗,且實驗中始終保持銅電極和碳鋼電極之間的距離為1 cm。不同Cl-濃度下T2銅合金和Q235鋼耦合后碳鋼表面的電偶電流密度(Ig,電偶電流與碳鋼表面積的比值)和耦合后的電偶電壓(Eg)如圖4和圖5所示。除了Cl-濃度外,還研究了溫度和銅合金/碳鋼面積比對電偶腐蝕的影響。實驗在數(shù)據(jù)穩(wěn)定至少10 h后停止測試,每個實驗時間為2~5 d。如圖4a,電偶對面積比為200∶1時的Ig明顯大于電偶對面積比為10∶1時的Ig,說明電偶腐蝕速率與銅合金的面積有關,受陰極反應控制。在T2銅合金和Q235鋼組成的電偶對中,T2銅合金表面主要發(fā)生O2的還原反應,Q235鋼作為陽極主要發(fā)生Fe的氧化。因此,在電偶腐蝕中,O2在銅合金表面的還原反應為速度控制步驟。面積比增大時,更多O2可以在銅合金表面還原,陰極電流增加,在電偶腐蝕中陰極陽極電流保持相等,所以當陽極面積相對較小時,Ig增大。
圖4
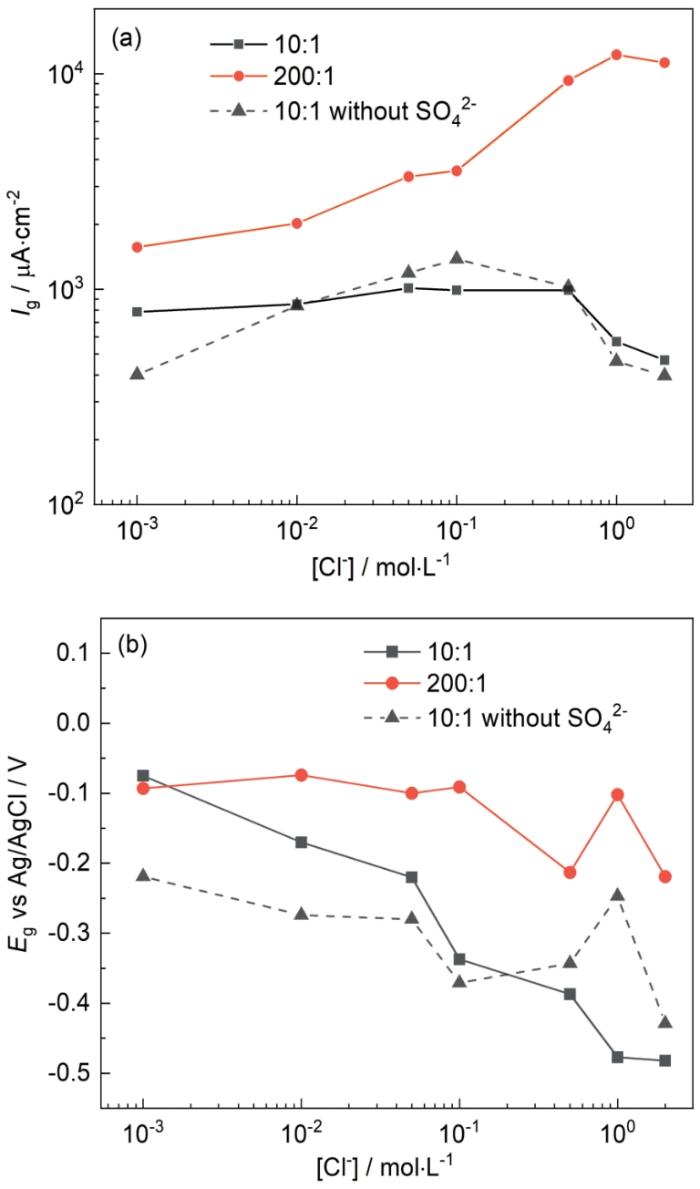
圖4 25℃時Cl-濃度對碳鋼表面電偶電流密度和電偶電壓的影響
Fig.4 Influences of Cl- concentration on galvanic current density (a) and galvanic potential (b) of Q235 steel at 25oC
圖5
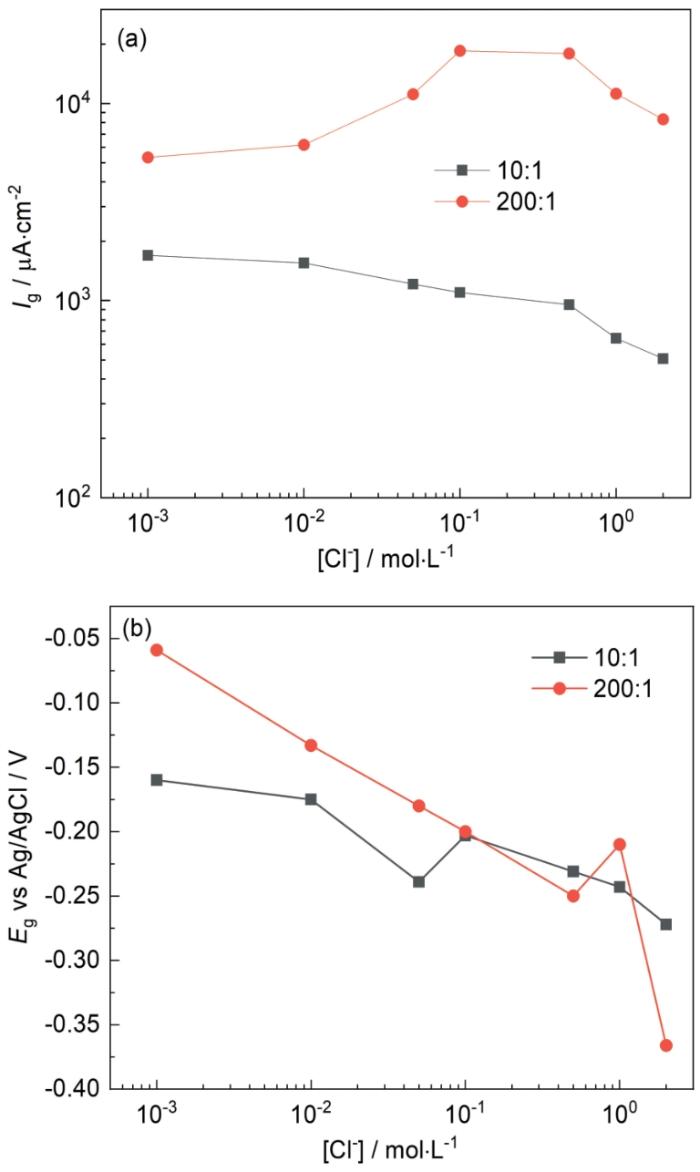
圖5 50℃時Cl-濃度對碳鋼表面的電偶電流密度和電偶電壓的影響
Fig.5 Influences of Cl- concentration on galvanic current density (a) and galvanic potential (b) of Q235 steel at 50oC
在溶液中隨著Cl-濃度增大,溶液中O2的溶解度降低。有文獻指出在22℃時,O2在0.1 mol·L-1 NaCl溶液中的溶解度為在3 mol·L-1 NaCl溶液中的2.7倍[23];在25℃時,O2在1 mol·L-1 NaCl溶液中的溶解度為在2 mol·L-1 NaCl溶液中的1.4倍,且O2溶解度降低的速率隨Cl-濃度增大變緩[24],溶解O2的降低會導致溶液中的氧濃度梯度下降,減少O2到銅合金表面的擴散通量,影響O2在銅合金表面的還原速率,進而降低電偶腐蝕速率。有文獻也指出NaCl溶液中隨Cl-濃度增大,O2的擴散系數(shù)會減小[25],進而降低O2到銅合金表面的擴散通量。其次,Cl-濃度變化還會影響溶液的電導率,如圖6所示,在25℃,溶液中含有0.015 mol·L-1 Na2SO4,Cl-濃度為0.01、0.1和1 mol·L-1時,溶液電導率分別為2540、6900、42600 μS·cm-1,溶液電導率隨Cl-濃度增大而增加,電導率的增加使溶液電阻下降,同時也加速了金屬表面鈍化膜的破裂,加快陽極溶解過程,導致電偶腐蝕速率加快。因此,在溶解氧和溶液電導率的相互影響下,Ig不會隨著Cl-濃度的增大持續(xù)增大,而是存在最大值。Eg的負移可能與溶液中溶解氧的減少有關,且Eg值更靠近T2銅合金的Ecorr,這也表明了在電偶腐蝕中反應受陰極的控制。
圖6
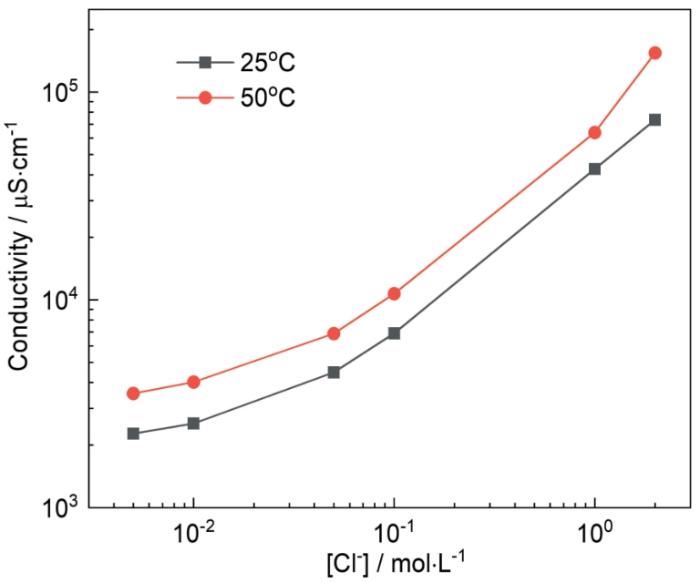
圖6 不同溫度下實驗溶液電導率隨Cl-濃度的變化
Fig.6 Variations of electrical conductivity of the test solution with Cl- concentration at 25oC and 50oC
Standish等[20]研究表明,當銅合金和碳鋼的面積比為10∶1時,Ig 在Cl-濃度為0.01~0.1 mol·L-1時出現(xiàn)最大值,這與本文的結果基本對應。但是當溶液中加入0.015 mol·L-1 Na2SO4,電偶對面積為10∶1時,Ig 隨Cl-濃度增大變化不明顯,這表明
50℃時Cl-濃度對Ig的影響如圖5a所示。面積比為10∶1時,Ig的數(shù)值均大于25℃時測得的數(shù)值,且Ig的最大值出現(xiàn)在Cl-濃度為0.001 mol·L-1時,隨Cl-濃度增大,Ig逐漸降低,在2 mol·L-1時兩個溫度下的Ig值僅相差39.6 μA·cm-2;面積比為200∶1時,Ig值在Cl-濃度低于0.5 mol·L-1時高于25℃時測得的數(shù)值,隨后Ig迅速減小最后在2 mol·L-1時為9309.2 μA cm-2,低于25℃時的11257.8 μA·cm-2。在圖5b中,Eg隨Cl-濃度增大負移,變化趨勢與25℃時相同。由圖5結果可以看出,溫度升高,會使Ig增大,即電偶腐蝕速率加快,這是因為溫度升高時,相同Cl-濃度下溶液電導率也隨之增大(圖6)。但溫度的升高也會引起溶液中溶解O2的減少,在常壓下,20℃時O2在純水中的溶解度約為50℃時的1.5倍,30℃時O2在1 mol·L-1 NaCl溶液中的溶解度約為60℃時的1.6倍[26],且隨著Cl-濃度增大,溶液中的溶解O2也會減少,因此在50℃時,Ig出現(xiàn)最大值時的Cl-濃度更低。
2.4 腐蝕產(chǎn)物分析
圖7為在25℃、面積比為10∶1時,Q235鋼在Cl-濃度分別為0.001、0.05和2 mol·L-1溶液中進行電偶腐蝕48 h后的SEM形貌圖。不同Cl-濃度下腐蝕形貌基本一致,腐蝕產(chǎn)物均勻分布在碳鋼表面,可分為內(nèi)、外兩層,內(nèi)層腐蝕產(chǎn)物較致密,外層腐蝕產(chǎn)物呈絮狀。其中,Cl-濃度為0.05 mol·L-1時(圖7c和d),碳鋼表面外層絮狀腐蝕產(chǎn)物最多,且聚集在一起;而Cl-濃度為0.001 mol·L-1(圖7a和b)和2 mol·L-1(圖7e和f)時,外層絮狀腐蝕產(chǎn)物減少,且沒有出現(xiàn)聚集。圖7中的腐蝕產(chǎn)物表面出現(xiàn)裂痕是因為在進行脫水干燥時腐蝕產(chǎn)物表面破裂所致。SEM形貌圖所示的表面腐蝕情況表明了在Cl-濃度為中等濃度時,腐蝕最嚴重,這與電偶腐蝕電化學測試結果相對應。
圖7
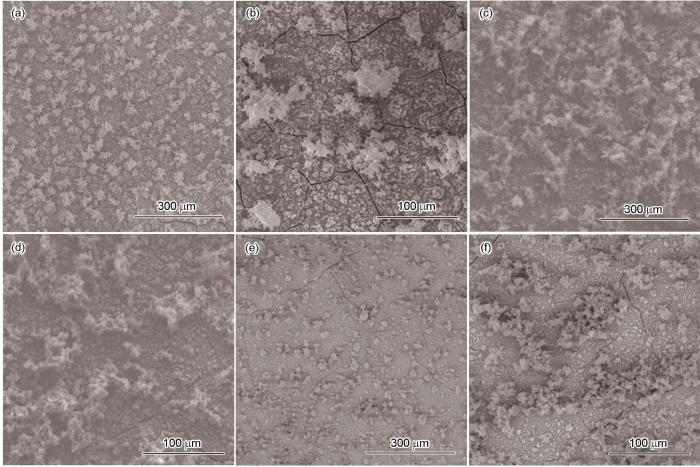
圖7 25℃時不同Cl-濃度下面積比為10∶1時Q235鋼表面腐蝕后SEM形貌圖
Fig.7 SEM surface morphologies of Q235 steel after corrosion at 25oC under the conditions of the area ratio of 10∶1 and Cl- concentrations of 0.001 mol·L-1 (a, b), 0.05 mol·L-1 (c, d), and 2 mol·L-1 (e, f)
圖8為Q235鋼在25℃下面積比為10∶1以及Cl-濃度為0.05 mol·L-1條件下溶液中電偶腐蝕48 h后的表面Raman光譜測試結果,分別對內(nèi)層和外層進行測試。如圖8a和b所示,內(nèi)層腐蝕產(chǎn)物在257 cm-1檢測到明顯的纖鐵礦γ-FeOOH[27]的特征Raman峰,在307、387 cm-1處檢測到明顯的針鐵礦α-FeOOH[28,29]的特征Raman峰,在1318 cm-1處檢測到少量α-Fe2O3[30]的特征峰;在535 cm-1處可見磁鐵礦Fe3O4[30]的特征Raman峰;在外層,如圖8c,d所示,腐蝕產(chǎn)物主要為α-Fe2O3[31],其特征Raman峰位于231、297、412、500、612和1324 cm-1處,此外還有α-FeOOH和少量位于670 cm-1處的Fe3O4特征Raman峰。在Raman測試的結果中并未發(fā)現(xiàn)Fe的氯化物的特征Raman峰,可能因為Cl-濃度較低和測試時間較短,F(xiàn)e的氯化物沒有在碳鋼表面沉積,也有研究表明Cl-在溶液中可以通過促進陽極溶解來加速腐蝕,生成的FeCl2不穩(wěn)定容易被氧化成FeOOH,Cl-又重新釋放回溶液中[32],在這個過程中Cl-起到某種催化劑的作用。從Raman測試結果可以看出,在電偶腐蝕中,陽極發(fā)生溶解后會先生成γ-FeOOH,由于γ-FeOOH不穩(wěn)定,容易被轉(zhuǎn)化成比較穩(wěn)定的α-FeOOH,當腐蝕產(chǎn)物暴露在空氣中時生成更穩(wěn)定的α-Fe2O3;而當腐蝕產(chǎn)物形成后內(nèi)層由于氧氣減少,F(xiàn)eOOH會部分轉(zhuǎn)化成Fe3O4,腐蝕產(chǎn)物會減緩碳鋼基體的腐蝕速率,因此在進行電偶腐蝕測試時總是觀察到Ig隨測試時間的進行逐漸變小直至穩(wěn)定。
圖8
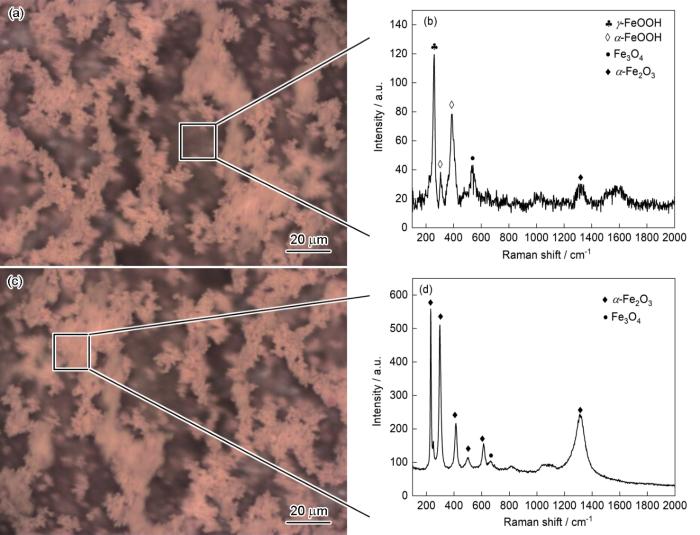
圖8 Q235鋼在25℃下面積比為10∶1以及Cl-濃度為0.05 mol·L-1條件下溶液中電偶腐蝕48 h后的表面Raman光譜
Fig.8 Raman spectra of inner layer (a, b) and out layer (c, d) of corrosion products formed on Q235 steel after galvanic corrosion, at 25oC with [Cl-] = 0.05 mol·L-1, Cu/carbon steel area ratio = 10∶1
3 結論
(1) OCP測試結果表明,在簡化版北山地下水模擬液中T2銅合金和Q235鋼接觸會發(fā)生嚴重電偶腐蝕,T2銅合金為陰極受到保護,Q235鋼為陽極腐蝕速率加速;隨Cl-濃度增大OCP差值減小,耦合效應可能減弱。
(2) 極化曲線測試結果表明,T2銅合金和Q235鋼陰極極化均受氧擴散控制,陽極極化為金屬的活性溶解,隨Cl-濃度增大T2銅合金陽極極化存在鈍化現(xiàn)象;T2銅合金的自腐蝕速率遠低于Q235鋼,銅鍍層良好的耐蝕性可以有效延長金屬儲罐的使用壽命。
(3) 電偶腐蝕實驗表明,T2銅合金和Q235鋼之間發(fā)生的電偶腐蝕受陰極O2的還原反應控制;隨Cl-濃度增大,溶液中溶解O2含量降低、氧擴散系數(shù)減小、電導率升高等因素使得Ig存在最大值,且溫度升高時,Ig在Cl-濃度更低時出現(xiàn)最大值,因此,在處置庫關閉初期的有氧高溫環(huán)境中,具有中等Cl-濃度的北山地下水模擬液對T2銅合金和Q235鋼的電偶腐蝕危害較大。
(4) 腐蝕產(chǎn)物分析結果表明,Q235鋼表面腐蝕產(chǎn)物分為較致密的內(nèi)層和成絮狀的外層,主要為Fe的羥基氧化物/氧化物。
免責聲明:本網(wǎng)站所轉(zhuǎn)載的文字、圖片與視頻資料版權歸原創(chuàng)作者所有,如果涉及侵權,請第一時間聯(lián)系本網(wǎng)刪除。

官方微信
《腐蝕與防護網(wǎng)電子期刊》征訂啟事
- 投稿聯(lián)系:編輯部
- 電話:010-62316606
- 郵箱:fsfhzy666@163.com
- 腐蝕與防護網(wǎng)官方QQ群:140808414