NH4H2PO4作為一種高效的復合肥料和工業原料,市場前景廣闊。目前,NH4H2PO4主要是以熱法磷酸或濕法磷酸與氨反應制得,其生產過程中會產生大量的低溫余熱[1,2]。低溫余熱資源回收利用的途徑主要為用作一般加熱熱源,被熱泵回收利用,低溫余熱發電[3]。隨著我國對低溫余熱發電的大力支持,再加上其自身具有顯著的經濟效益和社會效益,低溫余熱發電受到諸多青睞[4]。
低溫余熱發電技術的核心原理為有機朗肯循環 (ORC),低溫余熱發電裝置主要由循環泵、蒸發器、汽輪機、冷凝器四部分組成[3]。蒸汽在汽輪機中做完功后,其壓力和溫度不斷降低,并在汽輪機轉動部件 (如轉子) 表面形成較薄的液膜,由于低溫余熱發電裝置中無除氧、除鹽等設施,蒸汽中氧氣、腐蝕性雜質鹽等又會溶于薄液膜中而形成強電解質溶液,誘發轉子材料發生腐蝕破壞,給低溫余熱發電裝置的運行帶來安全隱患[4]。
目前,關于轉子材料的腐蝕研究,更多集中于核電或火力發電汽輪機低壓轉子材料的腐蝕行為研究[5-12]。Luo等[5-7]利用U型試樣研究了核電汽輪機焊接轉子25Cr2Ni2MoV焊接接頭在180 ℃、3.5% NaCl溶液中的腐蝕行為,研究表明,焊縫區優先產生大量夾雜物誘發的點蝕坑,此外,焊接接頭的母材、焊縫、熱影響區存在電勢差,并誘發電偶腐蝕。歐陽玉清等[8]研究了溫度對核電汽輪機焊接轉子25Cr2Ni2MoV焊接接頭電偶腐蝕的影響,研究表明,隨著溫度升高,材料電偶腐蝕效應增強。Maeng等[9]通過恒速率拉伸實驗研究了高溫水中醋酸對火力發電汽輪機低壓轉子材料3.5NiCrMoV應力腐蝕行為的影響,研究表明,隨著醋酸濃度增大,材料的應力腐蝕敏感性增大,此外,高濃度的醋酸也會造成裂紋尖端鈍化。與核電或火力發電汽輪機所用的蒸汽不同,利用NH4H2PO4生產行業產生的低溫余熱資源發電的裝置所用蒸汽溫度較低、壓力較小,造成轉子表面更容易形成一層薄液膜。正常情況下,核電或火力發電汽輪機中蒸汽的含氧量限制在5 10-3 mg/L以下,而啟停機時,從冷凝器進入的氧含量增大,最高氧含量可達20 mg/L,而低溫余熱發電裝置中無除氧設施,造成了其蒸汽中的氧含量遠高于核電或火力發電汽輪機所用的蒸汽[13]。低溫余熱發電裝置中也無除鹽設施,致使其蒸汽中還含有部分殘留的NH4H2PO4,NH4H2PO4易溶于水,形成酸性水溶液。然而,汽輪機轉子常見材料在含NH4H2PO4酸性溶液條件下NH4H2PO4溶液濃度等變化對材料腐蝕行為的影響規律及其機理鮮有報道,即NH4H2PO4溶液濃度、溶解氧、溫度等腐蝕因素影響的基礎研究尚未系統開展。
本文以2Cr-1Ni-1.2Mo-0.2V鋼作為研究對象,研究結果可為利用NH4H2PO4生產行業產生的低溫余熱資源發電的裝置開發及其防護提供理論依據和數據支持。
1 實驗方法
實驗用材為2Cr-1Ni-1.2Mo-0.2V鋼 (1R鋼),主要化學成分 (質量分數,%) 為:C 0.32,Si 0.02,Mn 0.6,S 0.0059,P 0.0015,Cr 2.23,Mo 1.17,Ni 0.95,V 0.22,Al 0.0058,Cu 0.048,As 0.006,Fe余量。1R鋼的組織以回火索氏體為主,同時還有少量塊狀的鐵素體組織。
實驗用溶液為不同濃度的NH4H2PO4溶液,即純度為99%的NH4H2PO4藥劑與去離子水混合而成的0 (純去離子水)、1、30、60、90、120 mmol/L NH4H2PO4溶液。
利用線切割的方式將實驗用材1R鋼加工成所需的試樣,失重實驗試樣規格為50 mm×20 mm×4 mm,XPS試樣規格為5 mm×5 mm×2 mm,電化學實驗試樣規格為10 mm×10 mm×10 mm。試樣加工后,認真清洗試樣表面的油污和鐵銹,電化學實驗試樣采用環氧樹脂對其進行真空冷鑲。隨后試樣表面逐級打磨至2000#水磨砂紙并最終拋光,拋光后,試樣在無水乙醇中超聲處理5 min,以去除試樣表面殘留的SiC顆粒,然后用去離子水清洗試樣表面,無水乙醇脫除殘留水分、冷風吹干,最后放入干燥器中待用,其中失重實驗試樣在干燥器中靜置24 h后稱重 (精確至0.1 mg)。去除失重實驗試樣腐蝕產物的酸洗液由500 mL鹽酸 (HCl, =1.19 g/mL)+5 g 1,3-二丁基-2-硫脲+500 mL去離子水配置而成。酸洗液去除腐蝕產物后,用去離子水、無水乙醇清洗試樣,冷風快速吹干,在干燥皿中靜置24 h后稱重 (精確至0.1 mg),并用 公式 (1) 計算材料腐蝕速率[14]。
(1)
其中,R均為腐蝕速率,g·m-2·h-1;M和Mt是實驗前和酸洗后的質量,g;S是試樣表面積,m2;T是實驗時間,h。
電化學實驗在PARSTAT4000型電化學工作站上進行,三電極體系,1R鋼為工作電極,鉑片為輔助電極,飽和甘汞電極 (SCE) 為參比電極,測試溫度為(25±2) ℃。開始測試前,試樣需在0 (純去離子水)、1、30、60、90、120 mmol/L NH4H2PO4溶液中浸泡20 h,待試樣表面穩定后再進行測試[15]。先測900 s開路電位,開路電位穩定后再進行相應的電化學測試,其中極化掃描在開路電位±0.25 V的范圍內進行,掃速為0.1666 mV/s;電化學阻抗譜 (EIS) 測試是在穩定的開路處對工作電極施加一個±5 mV的交流電壓擾動下進行的,測試頻率范圍為105~10-2 Hz,并使用ZSimDemo軟件對其數據進行擬合分析。
通過失重法測量1R鋼在不同濃度NH4H2PO4溶液中的腐蝕速率,利用LEXT-OLS5000激光共聚焦顯微鏡 (CLSM) 分析材料表面腐蝕形貌;選取在120 mmol/L NH4H2PO4溶液中浸泡20 h后的試樣,通過場發射掃描電鏡 (FE-SEM,Thermo Fisher APREO) 及其附帶的Quantax400能譜儀 (EDS) 分析內外層腐蝕產物形貌及其合金元素分布;在120 mmol/L NH4H2PO4溶液中浸泡20 h后的試樣表面刮取腐蝕產物粉末,使用X射線衍射儀 (XRD,Bruker D8 Advance) 對其進行物相分析,XRD測試采用Co靶,Kα波長0.15406 nm,管電壓40 kV,管電流為40 mA,掃描速度為20°/min,衍射角掃描范圍為10°~80°,使用MDI Jade6軟件處理數據;選取在30、60、90、120 mmol/L NH4H2PO4溶液中浸泡20 h后的試樣,用去離子水去除表面疏松的腐蝕產物,通過X射線光電子能譜儀 (XPS,AXIS ULTRADLD) 分析與1R鋼基體結合緊固的腐蝕產物組成,XPS測試所用光源為單色Al (=1486.6 eV),測試深度約5 nm,收集Fe 2p、Cr 2p、Mo 3d等能譜圖,通過C 1s (284.6 eV) 荷電校正后,采用XPS PEAK41軟件處理數據。
2 結果與討論
2.1 腐蝕速率
圖1為1R鋼在0 (去離子水)、1、30、60、90、120 mmol/L NH4H2PO4溶液中浸泡20 h的平均腐蝕速率。可見,1R鋼在去離子水中的腐蝕速率最小,約為0.017 g·m-2·h-1,在1 mmol/L NH4H2PO4溶液的腐蝕速率約為0.152 g·m-2·h-1,其值比1R鋼在去離子水中的腐蝕速率大7.973倍。繼續增大NH4H2PO4溶液的濃度,發現1R鋼的腐蝕速率也隨之增大。1~30、30~60、60~90、90~120 mmol/L NH4H2PO4溶液對應的1R鋼的腐蝕速率相對于NH4H2PO4溶液濃度的導數分別約為0.001、0.002、0.003、0.001 L·m-2·h-1 mmol-1,即隨著NH4H2PO4溶液濃度的增大,1R鋼的腐蝕速率先快速增大后緩慢增大。
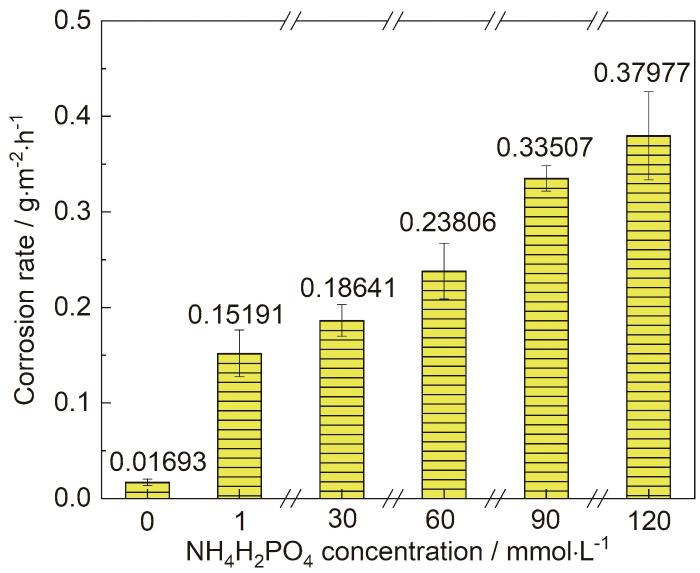
圖1 1R鋼在不同濃度NH4H2PO4溶液中浸泡20 h的平均腐蝕速率
2.2 腐蝕形貌及成分分析
圖2為1R鋼在0 (去離子水)、1、30、60、90、120 mmol/L NH4H2PO4溶液中浸泡20 h后的腐蝕形貌,圖2中所選區域的三維形貌見圖3。可見,1R鋼在去離子水和1 mmol/L NH4H2PO4溶液中浸泡20 h后,鋼基體表面均出現點蝕坑 (圖2a2和b2),從在這兩種溶液中浸泡后的試樣表面隨機選取2個點蝕坑,用激光共聚焦顯微鏡獲取其三維形貌 (見圖4a和b),可見1R鋼在去離子水中浸泡后而生成的點蝕坑孔徑和孔深分別為72.9和11.1 μm,而1R鋼在1 mmol/L NH4H2PO4溶液中浸泡后生成的點蝕坑孔徑和孔深分別73.5和3.1 μm,可見加入少量的NH4H2PO4,可明顯抑制點蝕坑向縱向發展。
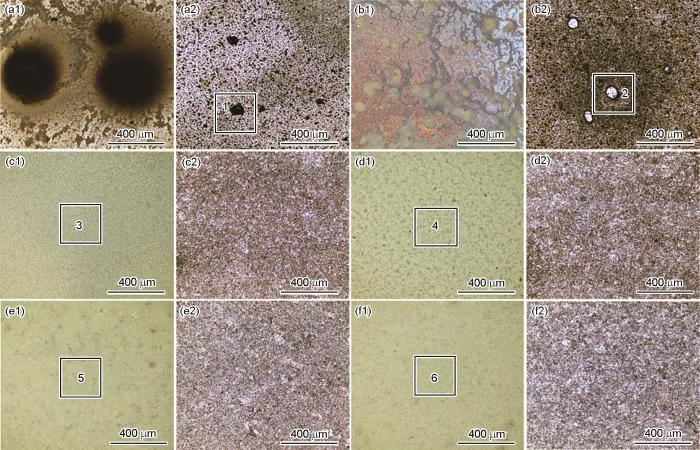
圖2 1R鋼在不同濃度NH4H2PO4溶液中浸泡20 h的表面腐蝕形貌
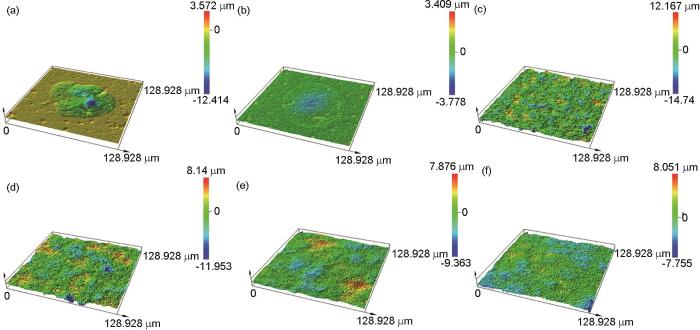
圖3 圖2中所選區域的三維形貌

圖4 在120 mmol/L NH4H2PO4溶液中浸泡20 h后的1R鋼試樣表面微觀形貌
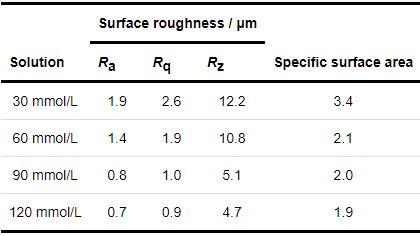
將1R鋼放入1 mmol/L NH4H2PO4溶液中浸泡20 h,發現材料表面被部分黃色腐蝕產物覆蓋,覆蓋度約15% (圖2b1)。當NH4H2PO4溶液濃度大于或等于30 mmol/L時,1R鋼表面均被黃色的腐蝕產物完全覆蓋 (圖2c1~f1)。利用激光共聚焦顯微鏡獲取1R鋼在30、60、90、120 mmol/L NH4H2PO4溶液中浸泡20 h后的表面三維形貌 (圖3c~f),可見材料表面的最大高度差分別為26.9、20.1、17.2和15.8 μm,說明隨著NH4H2PO4溶液濃度的增大,材料表面起伏程度逐漸減小。表1為1R鋼在30、60、90、120 mmol/L NH4H2PO4溶液中浸泡20 h后的表面粗糙度參數,可見表面粗糙度參數隨NH4H2PO4溶液濃度的增大而減小,這與上述表面起伏程度分析結果一致。隨著表面粗糙度的減小,表面積比參數也在減小,表明材料與腐蝕介質接觸的有效面積減小,此結果會抑制材料腐蝕速率增大[16]。
表1 1R鋼在30、60、90和120 mmol/L NH4H2PO4溶液中浸泡20 h后的表面粗糙度參數
1R鋼在30~120 mmol/L NH4H2PO4溶液中浸泡20 h后其表面覆蓋的黃色的腐蝕產物較為疏松,用鑷子輕輕剝落這些黃色的腐蝕產物,便可看到內部黑色的腐蝕產物。利用激光共聚焦顯微鏡測得剝落區相較于未剝落區的高度,本文將其高度近似等價于材料表面覆蓋的腐蝕產物膜厚度,表明1R鋼在30、60、90、120 mmol/L NH4H2PO4溶液中浸泡20 h后其表面覆蓋的厚度分別為8.7、10.6、14.8和18.6 μm,即隨著NH4H2PO4溶液濃度的增大,1R鋼表面覆蓋的腐蝕產物逐漸增厚。去除腐蝕產物膜后,在30、60、90、120 mmol/L NH4H2PO4溶液中浸泡20 h后的1R鋼基體均光滑平整,均未出現局部腐蝕,材料腐蝕特征為均勻腐蝕 (圖2c2~f2)。
為驗證1R鋼在30~120 mmol/L NH4H2PO4溶液中浸泡20 h后其表面形成的腐蝕產物膜為雙層結構,本文選取在120 mmol/L NH4H2PO4溶液中浸泡20 h后的1R鋼試樣,其表面微觀形貌見圖4。可見1R鋼試樣表面腐蝕產物膜為雙層結構,外層膜較為疏松 (圖4a),利用膠布將外層腐蝕產物膜輕輕粘除,可觀察到內層腐蝕產物膜 (圖4b),內層腐蝕產物膜較薄,可看到膜層下方鋼基體晶界,但內層膜致密度高于外層膜[17]。
為了進一步分析在120 mmol/L NH4H2PO4溶液中浸泡20 h后的1R鋼試樣表面內外層腐蝕產物膜的差異性,分別對內外層腐蝕產物膜進行EDS分析。由表2中EDS結果可知,外層腐蝕產物膜主要由O、P和Fe構成,Fe/P/O原子比為1.03∶1∶5.85,Fe含量為31.37% (質量分數),可推測外層腐蝕產物膜主要為鋼基體溶解生成的Fe2+及Fe3+ (溶液中的O將鋼基體溶解生成的Fe2+氧化為Fe3+) 與溶液中的陰離子 (如PO43-) 結合而形成的疏松膜層,再結合外層腐蝕產物膜中Fe/P/O原子比為1.03∶1∶5.85,說明該腐蝕產物膜層可能為一個FePO4和Fe3(PO4)2混合的膜層[18]。內層腐蝕產物主要由Fe、Cr、Mo、O和P構成,Fe/Cr/Mo原子比為101.95∶3.24∶1,Fe含量為88.70%,內層腐蝕產物中Fe含量約為外層腐蝕產物膜中Fe含量的2.83倍;P/O原子比為1∶10.37,可推測內層腐蝕產物膜主要為鋼基體與溶液中的O反應而生成的氧化物膜層[17]。
表2 在120 mmol/L NH4H2PO4溶液中浸泡20 h后的1R鋼試樣表面腐蝕產物EDS分析

為證實上述猜想,本文對在120 mmol/L NH4H2PO4溶液中浸泡20 h后的1R鋼表面生成的腐蝕產物進行XRD分析 (圖5)。由圖可知,有明顯的Fe3(PO4)2·8H2O衍射峰,該結果表明,腐蝕產物的主要成分有Fe3(PO4)2,反應過程中,鋼基體溶解生成的Fe2+與NH4H2PO4分解而成的PO43-結合并沉積在鋼基體上[18]。腐蝕產物的XRD圖譜也顯現出FePO4、Fe3O4衍射峰,結果表明,鋼基體溶解生成的Fe2+被溶液中的溶解氧氧化為Fe3+,該Fe3+與NH4H2PO4分解而成的PO43-結合并沉積在鋼基體上,另外,鋼基體與溶液中的O反應而生成FePO4。結合圖4,5和表2可知,1R鋼在120 mmol/L NH4H2PO4溶液中浸泡20 h后形成的腐蝕產物膜為雙層結構,外層腐蝕產物膜主要由Fe3(PO4)2、FePO4構成,內層腐蝕產物膜主要由Fe3O4構成,這與龍晉明等[19]的研究結果相似。
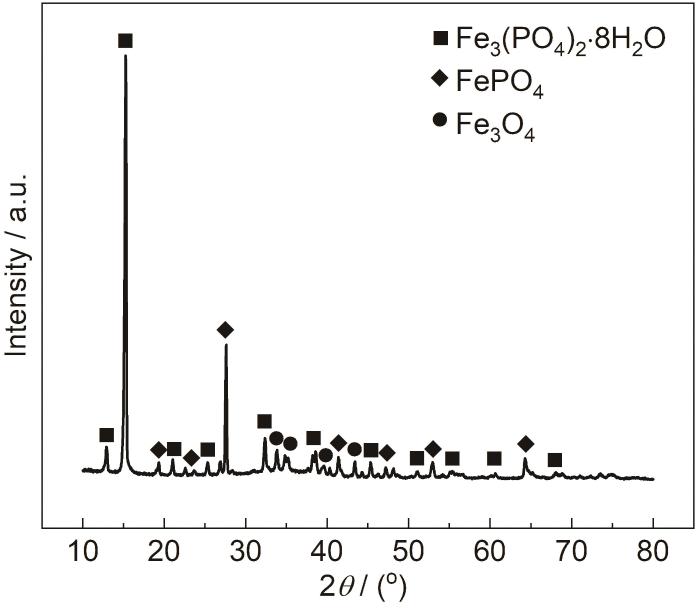
圖5 在120 mmol/L NH4H2PO4溶液中浸泡20 h后的1R鋼試樣表面腐蝕產物的XRD譜
2.3 XPS測試
通過上述分析,表明1R鋼在30~120 mmol/L溶液中浸泡20 h后形成的腐蝕產物膜為雙層結構,外層產物膜較疏松,且易脫落,而內層腐蝕產物膜附著力較強,因此本文用去離子水去除表面外層疏松的腐蝕產物,保留與基體結合緊固的內層腐蝕產物,并研究其相組成及其相對含量。
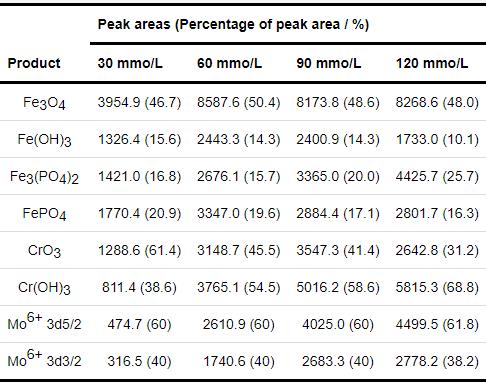
1R鋼在30~120 mmol/L NH4H2PO4溶液中浸泡20 h后形成的內層腐蝕產物膜中Fe 2p3/2、Cr 2p3/2、Mo 3d的XPS圖譜如圖6所示。通過NIST的原子譜數據庫和相關文獻對圖譜進行分峰擬合,主要組成物質的結合能分別為:Fe 2p3/2 Fe3O4/711.4 eV;Fe(OH)3/713.9 eV;Fe3(PO4)2/710.1 eV;FePO4/712.8 eV,Cr2p3/2 CrO3/578.3 eV;Cr(OH)3/577.1 eV,Mo 3d5/2 Mo6+/232.5 eV及Mo 3d3/2 Mo6+/235.8 eV。表3為XPS圖譜擬合出的峰面積及各峰的面積比[18-22]。可見內層腐蝕產物膜主要由Fe的氧化物、磷化物、氫氧化物,Cr的氧化物和氫氧化物及Mo6+的相應化合物組成。將NH4H2PO4溶液濃度由30 mmol/L提高到120 mmol/L,雖然溶液濃度增大了3倍,但是Fe3(PO4)2的峰面積比僅由16.8%增至25.7%,FePO4的峰面積比由20.9%減至16.3%,Fe(OH)3的峰面積比由15.6%減至10.1%,Fe3O4的峰面積比基本沒變,變化的原因是隨著NH4H2PO4溶液濃度的增大,溶液pH變小,從而抑制Fe2+氧化[23]。實驗表明30~120 mmol/L NH4H2PO4溶液中pH在4.1至4.9之間,接近FePO4沉淀產生的最佳pH (3~5),隨著Fe3+減少,FePO4的含量便會出現減少的趨勢,水解而得的Fe(OH)3也會出現減少的趨勢[24,25]。將溶液濃度由30 mmol/L提高到120 mmol/L,腐蝕產物膜中CrO3的峰面積比由31.2%增至61.4%,這或許是因為pH增大會促進穩定的Cr的氧化物生成[26]。
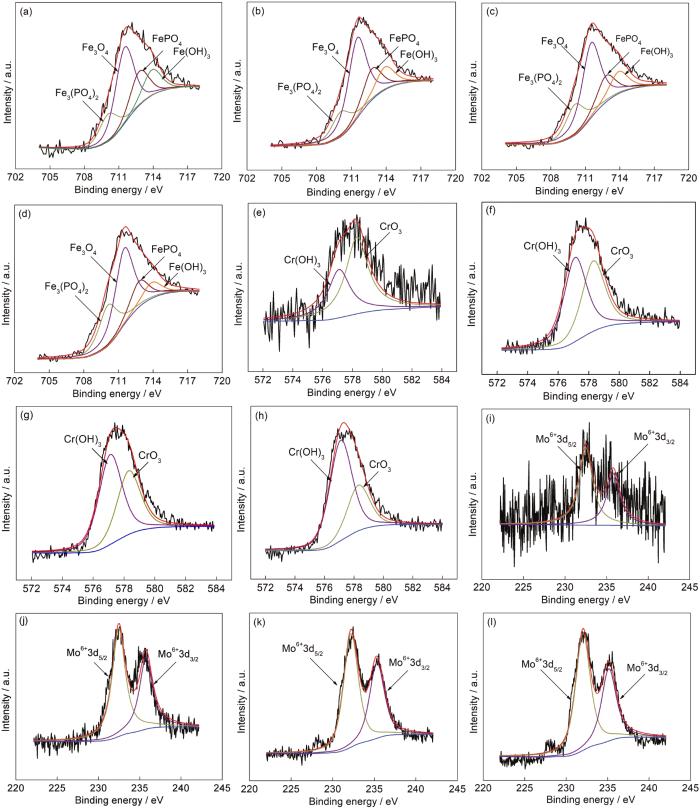
圖6 1R鋼在不同濃度NH4H2PO4溶液中形成的內層腐蝕產物膜中Fe 2p3/2,Cr2p3/2和Mo 3d XPS圖譜
表3 內層腐蝕產物膜中Fe 2p3/2、Cr 2p3/2、Mo 3d的XPS圖譜擬合出的峰面積及其所占的比重
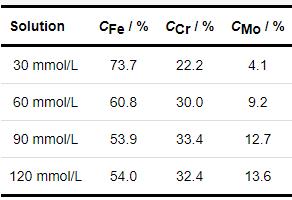
為了進一步分析1R鋼在30~120 mmol/L NH4H2PO4溶液中浸泡20 h后表面形成的內層腐蝕產物膜的差異性,本文利用 公式 (2) 計算不同濃度NH4H2PO4溶液對應的內層腐蝕產物膜中Fe、Cr、Mo之間原子分數 (Cx )[28]。其計算結果見表4。
表4 內層腐蝕產物膜中主要元素含量
(2)
其中,Ix 是各元素的峰強度,可用其對應的峰面積表示,Sx 為各元素的靈敏度因子,Fe 2p、Cr 2p、Mo 3d對應的靈敏度因子分別為2.957、2.427、3.321。從表5中可以看出,Fe對應的化合物為內層腐蝕產物膜中最主要的物質,隨著NH4H2PO4溶液濃度的增大,內層腐蝕產物膜中Fe含量呈下降趨勢,而Cr、Mo含量卻呈遞增趨勢。這是因為隨著NH4H2PO4溶液濃度的增大,溶液pH變小,電導率增大,內層腐蝕產物膜中Fe、Cr、Mo對應的化合物發生選擇性溶解,穩定性較差的Fe的氧化物、氫氧化物、磷化物溶解速度較快,而Cr的氧化物和氫氧化物及高價態Mo6+相應的化合物由于耐蝕性較好,溶解緩慢而出現一定的富集,從而造成內層腐蝕產物膜中Fe含量減少,而Cr、Mo含量增多的結果[27-30]。
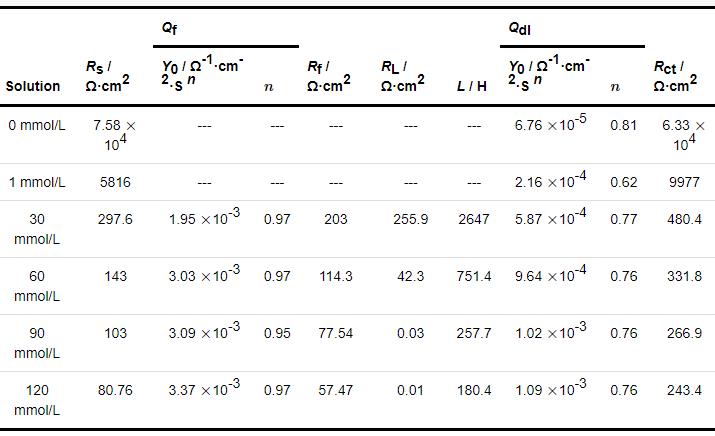
表5 1R鋼在不同濃度NH4H2PO4溶液中的電化學阻抗譜參數
2.4 開路電位
1R鋼在不同濃度NH4H2PO4溶液中浸泡20 h后測得的穩定開路電位,pH值和電導率如圖7所示。由圖7a可知,1R鋼的開路電位隨NH4H2PO4溶液濃度的增大先負移后基本不變,值得注意的是,1R鋼在30~120 mmol/L NH4H2PO4溶液中浸泡20 h后測得的開路電位極為相近 (圖7a)。實驗發現當溶液由去離子水變成30 mmol/L NH4H2PO4溶液時,溶液pH由6降到4.9,溶液電導率由0.6 μS/cm增到2695 μS/cm,電導率增大了約4491倍 (圖7b),隨著溶液pH快速下降,電導率快速上升,而此時1R鋼表面尚未形成致密的腐蝕產物膜,所以在此濃度范圍內,1R鋼的腐蝕傾向性隨NH4H2PO4溶液濃度的增大而增大,開路電位負移[32];將NH4H2PO4溶液濃度由30 mmol/L增大到120 mmol/L,溶液pH由4.9降到4.1,溶液電導率由2695 μS/cm增到8995 μS/cm電導率僅增大了約2.3倍;隨著NH4H2PO4溶液濃度的增大,試樣表面腐蝕產物形成也會加快,試樣表面覆蓋腐蝕產物逐漸增厚;內層腐蝕產物膜中Cr、Mo出現一定程度的富集 (表5),一定程度抑制1R鋼腐蝕,促進腐蝕因素與抑制腐蝕因素共同作用,最終造成了1R鋼的腐蝕傾向性基本不變的結果,故開路電位極為相近[30-33]。

圖7 1R鋼在不同濃度NH4H2PO4溶液中的開路電位及不同濃度NH4H2PO4溶液的pH和電導率
2.5 極化曲線
圖8為1R鋼在不同濃度NH4H2PO4溶液中浸泡20 h后從陰極向陽極方向進行掃描測試的Tafel曲線及其相應的自腐蝕電位和自腐蝕電流密度。由圖可見,自腐蝕電位隨NH4H2PO4溶液濃度的增大先負移后基本不變,其變化規律與上文開路電位分析結果一致。自腐蝕電位只是反映材料腐蝕的傾向,并不能說明材料腐蝕速率的大小,自腐蝕電流密度卻與材料腐蝕速率大小相關,一般材料自腐蝕電流密度越大,材料腐蝕越快[34,35]。從圖8b中可獲知1R鋼的自腐蝕電流密度隨NH4H2PO4溶液濃度的增大而增大,所以1R鋼的腐蝕速率隨NH4H2PO4溶液濃度的增大而增大。
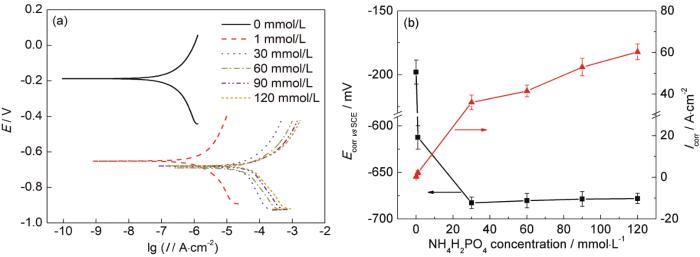
圖8 不同濃度NH4H2PO4溶液下1R鋼的極化曲線、自腐蝕電位和自腐蝕電流密度
2.6 電化學阻抗譜
圖9為1R鋼在不同濃度NH4H2PO4溶液中浸泡20 h后測得的電化學阻抗譜。從Nyquist圖可知,當NH4H2PO4溶液濃度為0~1 mmol/L時,電化學阻抗譜均有兩個容抗弧,相應的,在Bode圖 (圖9a4) 上有兩個時間常數,而高頻部分的容抗弧只有在低電導率溶液中才會出現,一旦溶液電導率增大到一定程度,高頻部分的容抗弧便消失不見 (圖9a2),由高頻部分的容抗弧擬合出來的電阻的倒數與溶液電導率呈線性關系[38]。隨著NH4H2PO4溶液濃度的增大,1R鋼試樣表面腐蝕產物增多,電化學阻抗譜表現為高頻區和低頻區各出現一個容抗弧 (圖9a2),其中高頻容抗弧與腐蝕產物膜的膜層電容及膜層電阻有關,而低頻容抗弧與雙電層電容及電荷轉移電阻有關,此外,低頻區也出現了感抗弧,相應的,在Bode圖 (圖9a4) 上還有一個低頻區的時間常數[17]。
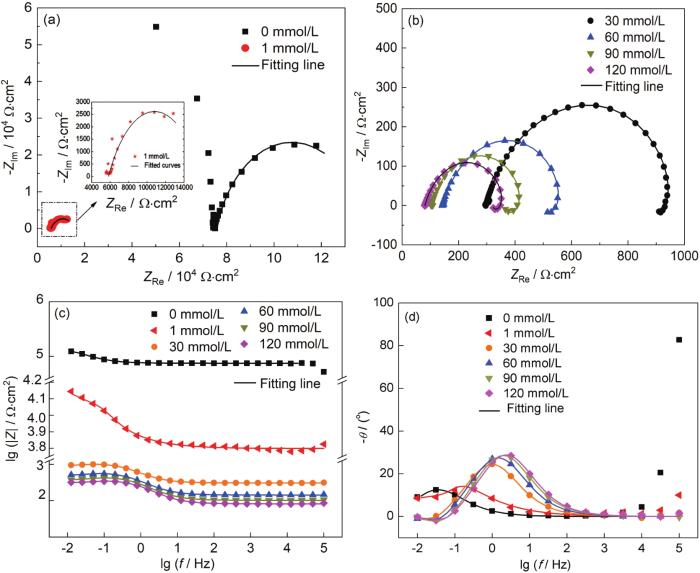
圖9 不同濃度NH4H2PO4溶液下1R鋼的電化學阻抗譜
結合圖2和4,給出了圖10所示的等效電路[37,39],擬合結果如表5所示。圖10a為1R鋼在0~1 mmol/L NH4H2PO4溶液中腐蝕的等效模型,此時1R鋼表面的腐蝕產物較少,其中,Rs為溶液電阻,Qdl為雙電層電容,Rct為電荷轉移電阻;圖10b為腐蝕產物完全覆蓋在1R鋼表面時的等效電路模型,其中,Rs為溶液電阻,Qf為腐蝕產物膜的膜層電容,Rf為膜層電阻,RL和L為感抗元件,感抗一般出現在腐蝕前期和后期,即尚未生成完整的保護膜層及后期部分膜層脫落時,通常,在局部電極表面出現腐蝕中間產物,Qdl為雙電層電容,Rct為電荷轉移電阻。其中,常相位角元件 的阻抗值可用 公式 (3) 計算[26]。
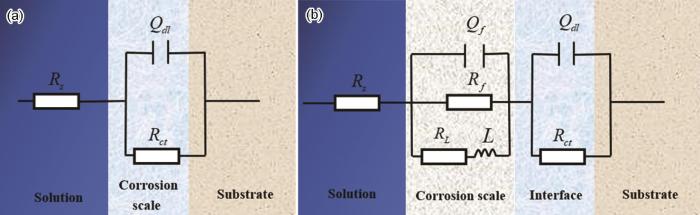
圖10 不同濃度NH4H2PO4溶液下1R鋼的等效電路
(3)
其中,ZQ為常相位角Q的阻抗值,Y0為導納模量,w為角頻率,j為虛數單位,n為彌散指數。
從表5中可知,去離子水的溶液電阻最大,其值為7.58 104 Ω·cm2,而上文中測得的去離子水的電導率為0.6 μS/cm,轉換為電阻率約為1.67 106 Ω·cm,造成電化學工作站測出來的溶液電阻偏小的原因是鹽橋中的KCl,鋼基體溶解生成的Fe2+等進入去離子水中,從而提高了溶液的導電性。將1、30、60、90、120 mmol/L NH4H2PO4溶液的導電率轉換為電阻率,其值分別為8961.9、371.1、199.5、139.4、111.2 Ω·cm,與電化學工作站測出來的溶液電阻值相近。此外,膜層電阻Rf、電荷轉移電阻Rct、感抗電阻RL均隨NH4H2PO4溶液濃度的增大而減小,而且電荷轉移電阻Rct隨NH4H2PO4溶液濃度的變化趨勢與上文腐蝕速率分析結果一致。
1R鋼試樣的電極反應為:

其中,陽極反應為金屬基體中鐵的溶解,而陰極反應為氧的去極化反應,部分Fe2+也會被溶液中的溶解氧氧化為Fe3+,隨著腐蝕過程的進行,H+、Fe2+、Fe3+、NH4+等向陰極區方向移動,而OH-、H2PO4-、HPO42-、PO43-等向陽極區方向移動,并在活化陽極區附近形成較為穩定的Fe(OH)3、FePO4、Fe3(PO4)2腐蝕產物[17,18]。
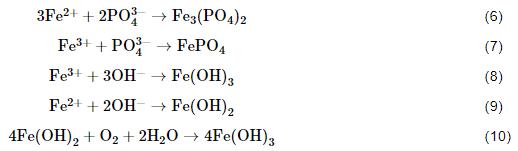
隨著NH4H2PO4溶液濃度的增大,1R鋼試樣表面形成的腐蝕產物膜覆蓋程度及致密程度均有所提高,內層腐蝕產物膜中Cr、Mo出現一定程度的富集,抑制了1R鋼腐蝕,但在所研究的濃度范圍內,溶液pH下降、電導率增大、材料表面形成的銹層疏松等促進材料腐蝕的因素處于主導地位,所以1R鋼的腐蝕速率隨NH4H2PO4溶液濃度的增大而增大,不過隨著NH4H2PO4溶液濃度的增大,抑制材料腐蝕的因素逐漸增強,從而造成1R鋼的腐蝕速率隨NH4H2PO4溶液濃度的增大先快速增大后緩慢增大的結果。這與上文腐蝕速率分析、形貌觀察結果一致。
3 結論
(1) 2Cr-1Ni-1.2Mo-0.2V鋼在去離子水中浸泡20 h后的平均腐蝕速率約為0.017 g·m-2·h-1,在1 mmol/L NH4H2PO4溶液中的腐蝕速率便增大7.973倍。1~30、30~60、60~90、90~120 mmol/L NH4H2PO4溶液對應的2Cr-1Ni-1.2Mo-0.2V鋼的腐蝕速率相對于NH4H2PO4溶液濃度的導數分別約為0.001、0.002、0.003、0.001 L·g·m-2·h-1 mmol-1,即隨著NH4H2PO4溶液濃度的增大,2Cr-1Ni-1.2Mo-0.2V鋼的腐蝕速率先快速增大后緩慢增大
(2) 2Cr-1Ni-1.2Mo-0.2V鋼僅在低濃度NH4H2PO4溶液中萌發點蝕,溶液濃度大于或等于30 mmol/L后,材料腐蝕形態表現為均勻腐蝕。2Cr-1Ni-1.2Mo-0.2V鋼表面腐蝕產物膜為雙層結構,外層腐蝕產物膜疏松,且易脫落,主要由Fe3(PO4)2、FePO4組成,而內層腐蝕產物膜附著力較強,主要由Fe3O4構成。隨著NH4H2PO4溶液濃度的增大,外層腐蝕產物膜覆蓋程度及致密程度均有所提高,內層腐蝕產物膜中Cr、Mo出現一定程度的富集,抑制了2Cr-1Ni-1.2Mo-0.2V鋼的腐蝕。
(3) 在0~120 mmol/L NH4H2PO4溶液中,隨著NH4H2PO4溶液濃度的增大,2Cr-1Ni-1.2Mo-0.2V鋼的穩定開路電位和自腐蝕電位均先負移后基本不變,而自腐蝕電流密度逐漸增大、電荷轉移傳遞電阻逐漸減小,即2Cr-1Ni-1.2Mo-0.2V鋼的腐蝕速率隨NH4H2PO4溶液濃度的增大而增大。
參考文獻:
略
免責聲明:本網站所轉載的文字、圖片與視頻資料版權歸原創作者所有,如果涉及侵權,請第一時間聯系本網刪除。

官方微信
《腐蝕與防護網電子期刊》征訂啟事
- 投稿聯系:編輯部
- 電話:010-62316606-806
- 郵箱:fsfhzy666@163.com
- 腐蝕與防護網官方QQ群:140808414





