摘要
采用分子動(dòng)力學(xué)模擬技術(shù)對(duì)CO2/H2S腐蝕體系中咪唑啉季銨鹽 (IAS) 與3種陽離子表面活性劑間的緩蝕協(xié)同效應(yīng)進(jìn)行了預(yù)測(cè),并通過失重法、極化曲線測(cè)試、XPS分析等對(duì)預(yù)測(cè)結(jié)果進(jìn)行驗(yàn)證,同時(shí)探討了緩蝕協(xié)同機(jī)理。結(jié)果表明,IAS與十二烷基三甲基溴化銨 (DTAB)、十四烷基三甲基溴化銨 (TTAB) 間存在較好的緩蝕協(xié)同效應(yīng),所形成的復(fù)合緩蝕劑屬于以抑制陽極為主的混合型緩蝕劑;XPS分析結(jié)果表明,復(fù)合緩蝕劑中起主要緩蝕作用的物質(zhì)可能為IAS,而表面活性劑則起到填補(bǔ)緩蝕劑膜層缺陷的作用,不同復(fù)配體系協(xié)同效應(yīng)的差異,可能與緩蝕劑分子的空間位阻有關(guān)。
關(guān)鍵詞: CO2/H2S腐蝕 ; 碳鋼 ; 緩蝕劑 ; XPS ; 分子動(dòng)力學(xué)模擬 ; 自由體積分?jǐn)?shù)
CO2/H2S引起的碳鋼腐蝕是油氣田行業(yè)中常見的腐蝕類型,由其引發(fā)的事故屢見不鮮。抑制CO2/H2S腐蝕的方法有很多,其中加注緩蝕劑是一種操作簡(jiǎn)單、經(jīng)濟(jì)有效的腐蝕防護(hù)手段,目前已得到廣泛應(yīng)用。單一的緩蝕劑在實(shí)際應(yīng)用中一般無法滿足設(shè)備設(shè)施的防腐需求,此時(shí)可利用兩種或多種緩蝕劑間的協(xié)同效應(yīng)來制備復(fù)合緩蝕劑,在降低成本的同時(shí)提高了緩蝕劑的性能[1]。
雖然緩蝕協(xié)同效應(yīng)相關(guān)研究已取得長(zhǎng)足進(jìn)展,產(chǎn)生了包括架橋理論[2,3,4,5,6,7]、補(bǔ)強(qiáng)理論[8,9]、協(xié)同吸附理論[10,11]等在內(nèi)的緩蝕協(xié)同效應(yīng)理論,但整體來說,協(xié)同效應(yīng)的研究多數(shù)還集中在無機(jī)酸性體系 (如HCl,H2SO4,H3PO4)[1,6,7,12,13,14,15]或CO2腐蝕體系[8,11],在CO2/H2S共存的鹽水溶液中,相關(guān)報(bào)道較少。
此外,之前對(duì)協(xié)同效應(yīng)的研究往往依賴于大量的實(shí)體實(shí)驗(yàn),如失重法、電化學(xué)測(cè)試、表面分析等,這些方法只能在宏觀上研究緩蝕劑間的協(xié)同效應(yīng),較難從微觀上解釋協(xié)同機(jī)理,且實(shí)驗(yàn)過程缺乏一定的理論指導(dǎo)。分子模擬技術(shù)目前已成為研究微觀機(jī)理的有效手段,并已被眾多學(xué)者用來評(píng)估緩蝕劑的性能[16,17,18,19,20,21,22,23]。本課題組首次將分子模擬技術(shù)應(yīng)用于緩蝕協(xié)同效應(yīng)的研究,并取得一定進(jìn)展[24],但這方面的報(bào)道依然較少。
本文采用分子模擬技術(shù)研究了IAS與3種陽離子表面活性劑間的緩蝕協(xié)同效應(yīng),發(fā)現(xiàn)IAS與DTAB和TTAB間可能存在協(xié)同效應(yīng);進(jìn)而通過靜態(tài)失重、極化曲線、XPS等方法對(duì)緩蝕劑間的協(xié)同效應(yīng)進(jìn)行驗(yàn)證,并探討了緩蝕協(xié)同機(jī)理。此外,本文的研究成果證明了課題組在文獻(xiàn)[24]中提出的方法在一定程度上可以預(yù)測(cè)緩蝕劑間協(xié)同效應(yīng),有繼續(xù)深入研究的價(jià)值。
1 實(shí)驗(yàn)方法
1.1 實(shí)驗(yàn)材料
實(shí)驗(yàn)中所用腐蝕試片為Q235鋼,化學(xué)成分 (質(zhì)量分?jǐn)?shù),%) 為:C 0.12-0.20,Si 0.10-0.25,Mn 0.30~0.70,P<0.045,S<0.045,Cu<0.15,Al<0.020,F(xiàn)e余量。實(shí)驗(yàn)前將鋼片切割成50×10×3 mm用于失重實(shí)驗(yàn),10 mm×10 mm×3 mm用于電化學(xué)測(cè)試,5 mm×5 mm×2 mm用于XPS測(cè)試,用砂紙逐級(jí)打磨至2000#后,去污粉清洗,丙酮去脂,乙醇脫水,熱風(fēng)吹干后備用。
實(shí)驗(yàn)介質(zhì)為3.5% (質(zhì)量分?jǐn)?shù)) NaCl溶液,實(shí)驗(yàn)前通1 h N2除氧,除氧結(jié)束后繼續(xù)向溶液中通CO2/H2S混合氣體 (20:20 mL/min) 1 h,制備腐蝕溶液,60 ℃時(shí)腐蝕溶液的pH值約為4.1。咪唑啉季銨鹽 (IAS) 由北京龍飛恒信科技有限公司提供,純度為95%;3種陽離子表面活性劑分別是十二烷基三甲基溴化銨 (DTAB)、十四烷基三甲基溴化銨 (TTAB) 和十六烷基三甲基溴化銨 (CTAB),均為分析純。IAS與3種陽離子表面活性劑的分子結(jié)構(gòu)如圖1。
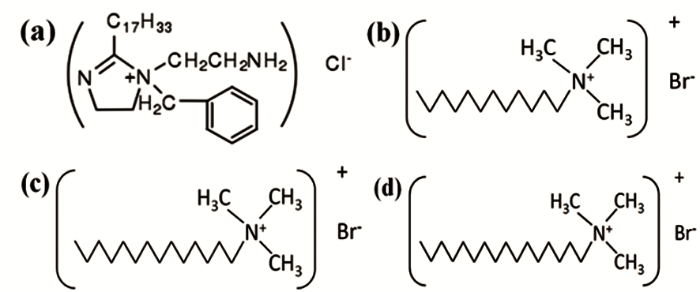
圖1 IAS與3種陽離子表面活性劑的分子結(jié)構(gòu)式
1.2 分子模擬
采用Material Studio中的Discover模塊構(gòu)建用于計(jì)算自由體積分?jǐn)?shù) (FFV) 的緩蝕劑膜模型并進(jìn)行分子動(dòng)力學(xué)模擬。模型包含一種或兩種緩蝕劑分子 (分子總個(gè)數(shù)為50)。計(jì)算過程中先進(jìn)行500 ps的NPT模擬用以計(jì)算緩蝕劑膜層的真實(shí)密度;之后用所得密度重新構(gòu)建模型,并進(jìn)行1000 ps的NVT模擬,NVT模擬后的終態(tài)結(jié)構(gòu)用于計(jì)算膜層FFV值。模擬過程采用Compass力場(chǎng);溫度為333 K (采用Andersen恒溫器控制);壓力為1.01×105 Pa (采用Berendsen恒壓器控制);長(zhǎng)程Coulomb力及van der Waals作用力分別采用Ewald和Atom Based,截?cái)喟霃綖?.25 nm。詳盡的模型構(gòu)建及模擬過程可參見本課題組前期工作[24]。FFV的計(jì)算公式如下:
![]()
其中,Vfree為腐蝕粒子能夠進(jìn)入的所有孔洞的體積;除Vfree外,剩余的體積為Voccupy。
1.3 靜態(tài)失重法
將稱重后3個(gè)相同的試片置于700 mL腐蝕溶液中,用704室溫固化硅橡膠封閉瓶口,并在60 ℃恒溫水浴鍋中保溫。72 h后,取出的試片先浸泡在酸洗液 (15%鹽酸+1%酸洗緩蝕劑) 中5 min,并用去污粉清洗,乙醇脫水,熱風(fēng)吹干后稱重。
1.4 動(dòng)電位極化曲線測(cè)試
在Gamry interface 1000電化學(xué)工作站上進(jìn)行電化學(xué)測(cè)試,采用傳統(tǒng)的三電極體系,參比電極和輔助電極分別為飽和甘汞電極 (SCE) 和Pt電極。測(cè)試前,需將工作電極浸泡在200 mL腐蝕溶液中1 h,使電極達(dá)到穩(wěn)定狀態(tài)。測(cè)試過程中,電位掃描范圍為-200~+200 mV,掃描速率0.167 mV·s-1。采用弱極化區(qū)三參數(shù)法對(duì)極化曲線進(jìn)行擬合,得到腐蝕電流密度 (Icorr) 等電化學(xué)參數(shù)進(jìn)行擬合,緩蝕率 (ηp) 可由下式計(jì)算:
![]()
其中,Icorr與Icorr (int) 分別為溶液中不含有和含有緩蝕劑時(shí)的自腐蝕電流密度值。
1.5 XPS測(cè)試
樣品制備過程與失重實(shí)驗(yàn)相同。試樣從腐蝕溶液中取出后,直接熱風(fēng)吹干,置于干燥器中備用。采用PHI-5300 ESCA光電子能譜儀 (XPS) 進(jìn)行能譜分析,掃描范圍為0~1255 eV,步長(zhǎng)1 eV,高分辨窄譜的掃描范圍與所測(cè)元素有關(guān),步長(zhǎng)為0.05 eV。XPS數(shù)據(jù)采用XPSPEAK軟件進(jìn)行擬合分析,分析過程中以C在284.6 eV處的結(jié)合能校準(zhǔn)其它結(jié)合能。
2 實(shí)驗(yàn)結(jié)果
2.1 分子動(dòng)力學(xué)模擬
有機(jī)緩蝕劑通常會(huì)自發(fā)地吸附在金屬表面來達(dá)到抑制金屬腐蝕的目的。雖然緩蝕劑膜層可以有效防止腐蝕介質(zhì)向金屬基體表面擴(kuò)散,但腐蝕介質(zhì)依然可以通過緩蝕劑膜中較大的孔洞[19],且孔洞越大,腐蝕粒子的擴(kuò)散速度就會(huì)越快。因此,緩蝕劑膜中孔洞的尺寸直接影響了緩蝕劑的性能。本課題組在分子動(dòng)力學(xué)模擬研究中發(fā)現(xiàn)[24],兩種緩蝕劑復(fù)配后對(duì)FFV值的降低程度與二者間的緩蝕協(xié)同效應(yīng)強(qiáng)度存在相關(guān)性。依據(jù)這一研究成果,本節(jié)以H2O、H3O+、HCO3-、Cl-和HS-為探針,計(jì)算了IAS與3種表面活性劑按一定質(zhì)量濃度比 (1∶0,1∶0.1,1∶0.2,1∶0.3,1∶0.4,1∶0.5,1∶0.7,1∶0.8,1∶1,1∶1.5,1∶2,1∶5,1∶8和0∶1) 復(fù)配后的緩蝕劑膜的FFV值,見圖2。可以看出,隨著探針直徑的增大,各緩蝕劑膜的FFV值也相應(yīng)減小,但無論使用何種探針,曲線的形狀均一致。
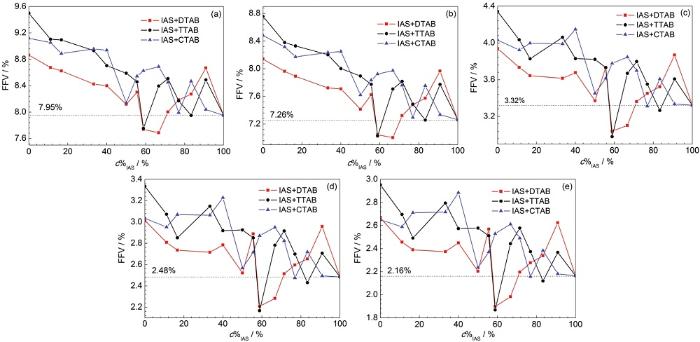
圖2 以H2O、H3O+、Cl-、HCO3-或HS-為探針時(shí)不同復(fù)合緩蝕劑膜層的FFV值隨c%IAS的變化曲線
對(duì)圖2a中3種復(fù)配體系的FFV計(jì)算結(jié)果進(jìn)行分析可以看出,與表面活性劑相比,IAS單獨(dú)成膜時(shí),緩蝕劑膜的FFV值更小,為7.95%;當(dāng)3種表面活性劑分別以不同比例與IAS混合時(shí),復(fù)合緩蝕劑膜層的FFV值出現(xiàn)了不同程度的變化:(1) 對(duì)于IAS+DTAB體系來說,當(dāng)IAS的質(zhì)量濃度在復(fù)合緩蝕劑中的占比 (c%IAS) 在65%附近時(shí),部分曲線在虛線下方,說明膜層的FFV值在這一區(qū)域內(nèi)低于7.95%,也就是說,IAS與DTAB復(fù)合使用,可以顯著增加膜層致密性,二者間可能存在較好的緩蝕協(xié)同效應(yīng);(2) 對(duì)于IAS+TTAB體系,當(dāng)c%IAS在60 %附近時(shí),有少部分曲線處于虛線下方,說明IAS與TTAB間也可能存在緩蝕協(xié)同效應(yīng),但協(xié)同強(qiáng)度小于IAS+DTAB體系;(3) 當(dāng)IAS與CTAB復(fù)合使用時(shí),曲線全部處于虛線上方,說明二者間可能存在拮抗效應(yīng)。
總之,根據(jù)分子動(dòng)力學(xué)模擬計(jì)算結(jié)果,推測(cè)IAS與DTAB、TTAB間存在協(xié)同效應(yīng),與CTAB間存在拮抗效應(yīng);協(xié)同效應(yīng)強(qiáng)度的排序?yàn)镈TAB+IAS> TTAB+IAS>CTAB+IAS。
2.2 失重實(shí)驗(yàn)結(jié)果
本節(jié)采用失重法對(duì)分子動(dòng)力學(xué)模擬的推測(cè)結(jié)果進(jìn)行驗(yàn)證。表1為靜態(tài)失重法實(shí)驗(yàn)結(jié)果。從表中可以看出,與3種表面活性劑相比,IAS對(duì)碳鋼的緩蝕效果更好。當(dāng)3種表面活性劑分別與IAS復(fù)配時(shí),復(fù)合緩蝕劑的性能排序?yàn)镮AS+DTAB>IAS+TTAB>IAS+CTAB。此外,5 mg/L IAS+5 mg/L DTAB和5 mg/L IAS+5 mg/L TTAB的復(fù)配組合,復(fù)合緩蝕劑的緩蝕率明顯大于分別使用5 mg/L單一緩蝕劑所得緩蝕率的和,即1+1>2,說明這兩種復(fù)配體系具有較好的緩蝕協(xié)同效應(yīng)。根據(jù)公式 (3) 可計(jì)算得到不同復(fù)配體系的S值,用以表明緩蝕劑間的協(xié)同效應(yīng)強(qiáng)度。
表1 不同緩蝕劑在含CO2/H2S鹽水中對(duì)Q235鋼的緩蝕效果
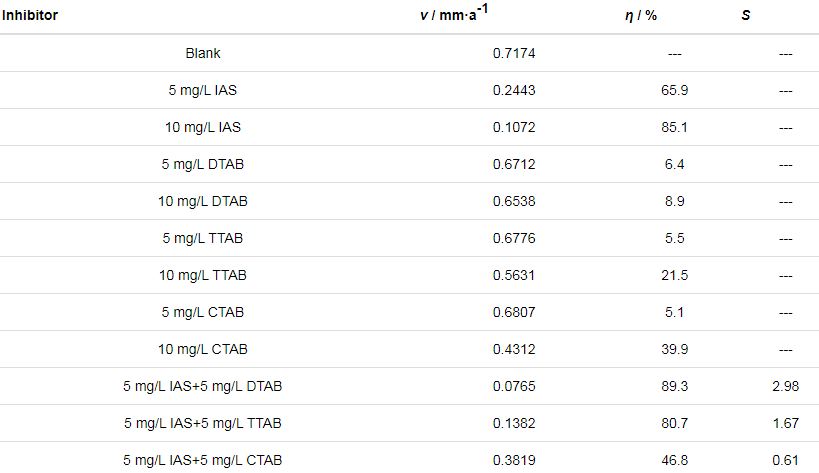
![]()
其中,ηA和ηB分別表示A與B各自單獨(dú)使用時(shí)測(cè)得的緩蝕率;ηAB表示A與B混合使用時(shí)測(cè)得的緩蝕率。若S值大于1,表明存在協(xié)同效應(yīng),S值越大,協(xié)同效應(yīng)越明顯。S值的計(jì)算結(jié)果列于表2中,可以看出,IAS與DTAB、TTAB間存在較好的緩蝕協(xié)同效應(yīng),與CTAB間存在拮抗效應(yīng);3種體系緩蝕協(xié)同效應(yīng)強(qiáng)度的排序?yàn)镮AS+DTAB>IAS+TTAB>IAS+CTAB。失重實(shí)驗(yàn)與分子動(dòng)力學(xué)模擬所得結(jié)論完全一致,說明考察不同緩蝕劑復(fù)合后對(duì)緩蝕劑膜FFV值的降低程度,可以在一定程度上預(yù)測(cè)緩蝕劑間的協(xié)同效應(yīng)。當(dāng)然,該方法的適用性還需要通過更多的研究進(jìn)行驗(yàn)證。
2.3 動(dòng)電位極化曲線測(cè)試
極化曲線實(shí)驗(yàn)主要是對(duì)失重結(jié)果的驗(yàn)證。圖3為Q235鋼在含有不同緩蝕劑的CO2/H2S共存鹽水溶液中測(cè)得的極化曲線。從圖中可以看出,緩蝕劑的加入對(duì)碳鋼陽極溶解和陰極反應(yīng)均有一定的影響,曲線均有向左上方移動(dòng)的趨勢(shì)。當(dāng)IAS與DTAB及TTAB復(fù)配使用時(shí),腐蝕電位明顯向正方向移動(dòng),而IAS與CTAB復(fù)配時(shí),腐蝕電位略微正移。無論怎樣,腐蝕電位的偏移程度均未超過85 mV,說明這些復(fù)合緩蝕劑均是以抑制陽極為主的混合型緩蝕劑[25,26]。

圖3 Q235鋼在含有不同緩蝕劑的CO2/H2S共存鹽水溶液中測(cè)得的極化曲線
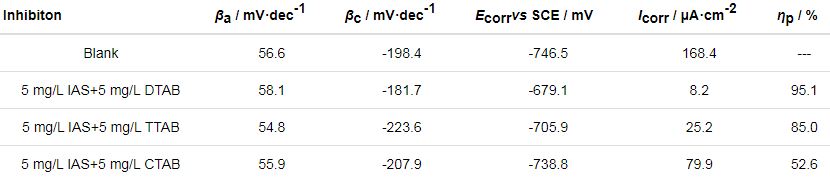
表2為對(duì)極化曲線進(jìn)行擬合后得到的電化學(xué)參數(shù),可以看出,IAS與DTAB或TTAB形成的復(fù)合緩蝕劑可有效抑制碳鋼在CO2/H2S溶液中的腐蝕,而IAS與CTAB復(fù)配形成的緩蝕劑緩蝕性能較弱。極化曲線與失重實(shí)驗(yàn)所得結(jié)論保持一致。
表2 通過擬合Q235鋼在含有不同緩蝕劑的CO2/H2S共存鹽水溶液中測(cè)得的極化曲線得到的電化學(xué)參數(shù)
2.4 XPS測(cè)試結(jié)果
為了進(jìn)一步研究IAS與3種表面活性劑間的緩蝕協(xié)同效應(yīng),本節(jié)采用XPS技術(shù)對(duì)帶有緩蝕劑膜的鋼片試樣進(jìn)行檢測(cè)分析。圖4為添加不同緩蝕劑時(shí)測(cè)得的緩蝕劑膜的XPS全譜。從圖中可以明顯地觀察到F2p、O1s、N1s、C1s、和S2p峰的存在。C1s和N1s主要來源于吸附在碳鋼表面的IAS和表面活性劑分子。O1s和S2p來自于鐵的氧化物、碳氧化物和硫化物。Fe2p則歸因于鐵基體和它的腐蝕產(chǎn)物。
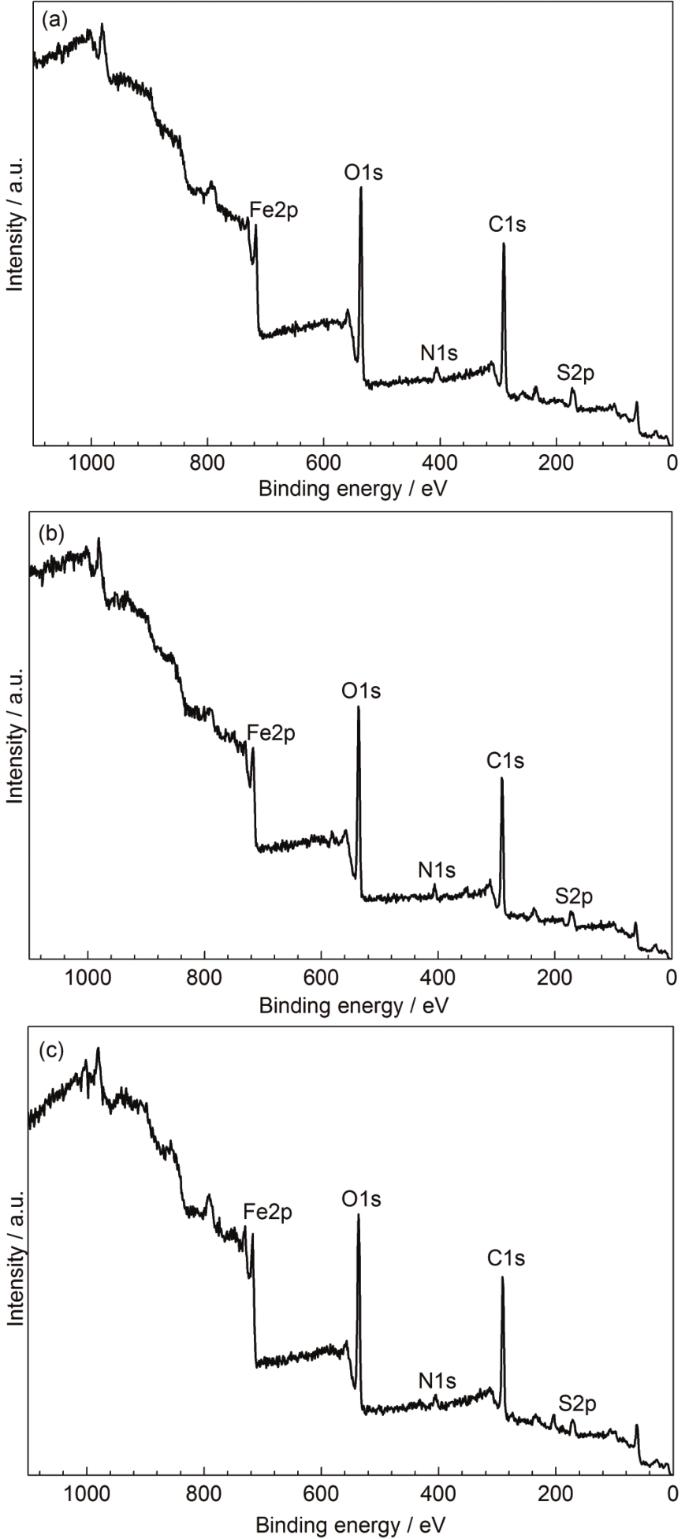
圖4 Q235鋼在含有不同緩蝕劑的CO2/H2S共存鹽水溶液中浸泡24 h后測(cè)得的XPS全譜
圖5為IAS與3種表面活性劑形成的緩蝕劑膜的N1s窄譜。圖5中的譜圖均可分解為位于402.3和399.8 eV處的兩個(gè)峰。402.3 eV處的峰源于表面活性劑中的—N+(CH3)3及IAS中季銨化后的N原子[27,28],這些N原子周圍均帶有一個(gè)正電荷,因此下文中將402.3 eV處的峰簡(jiǎn)稱為N+峰;而399.8 eV處的峰則歸屬于IAS中的C—N=C[29]。
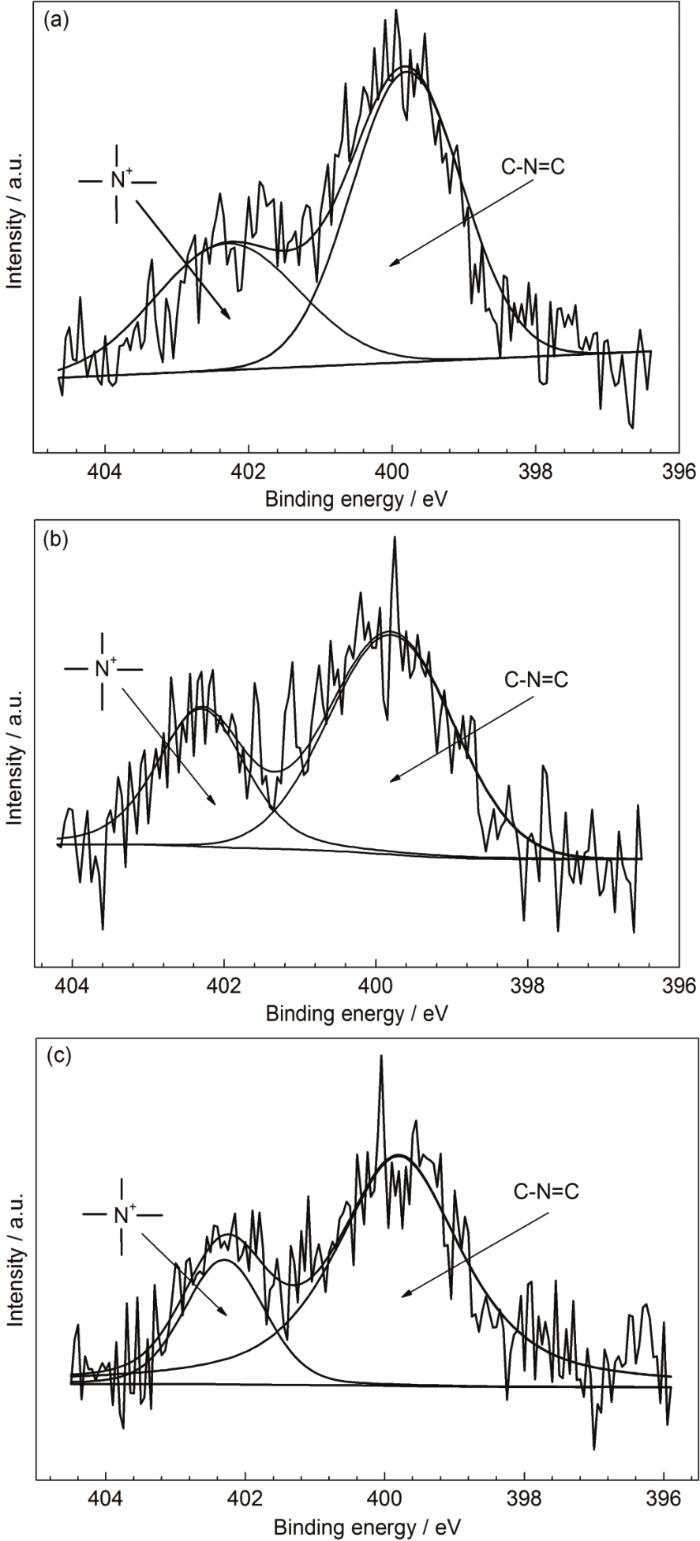
圖5 Q235鋼在含有不同緩蝕劑的CO2/H2S共存鹽水溶液中浸泡24 h后測(cè)得的N1s高分辨窄譜
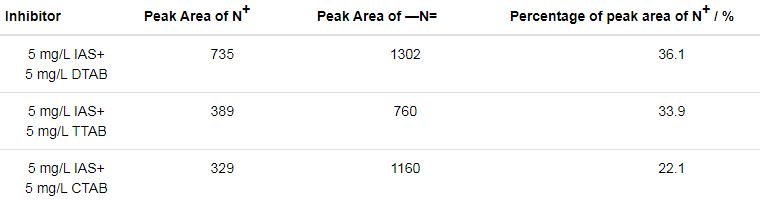
通過對(duì)N1s高分辨窄譜的擬合,可以得到N+及C—N=C峰的面積及N+峰面積的占比,見表3。可以看出,IAS與DTAB復(fù)配使用時(shí),N+峰面積的占比最大,說明緩蝕劑膜層中含表面活性劑 (DTAB) 的含量最多,證明了IAS與DTAB可以較好的共吸附在碳鋼表面。N+峰面積的占比排序?yàn)镮AS+DTAB>IAS+TTAB>IAS+CTAB,與緩蝕劑間協(xié)同效應(yīng)強(qiáng)度排序一致。
表3 通過分析Q235鋼在含有不同緩蝕劑的CO2/H2S共存鹽水溶液中浸泡24 h后測(cè)得的N1s高分辨窄譜得到的參數(shù)
3 緩蝕協(xié)同機(jī)理分析
從表3可知,IAS與3種表面活性劑復(fù)配時(shí),碳鋼表面IAS的含量明顯多于表面活性劑,而IAS的緩蝕性能卻好于表面活性劑,說明復(fù)合緩蝕劑中,起主要緩蝕作用的物質(zhì)可能為IAS,而表面活性劑則起到填補(bǔ)緩蝕劑膜層缺陷的作用。此外,雖然3種表面活性劑緩蝕性能的排序?yàn)镃TAB>TTAB>DTAB,但與IAS復(fù)配后,協(xié)同效應(yīng)強(qiáng)度的排序卻為IAS+DTAB>IAS+TTAB>IAS+CTAB,說明協(xié)同作用的強(qiáng)度可能與表面活性劑本身的性能差異無關(guān),而與緩蝕劑膜層的致密程度有關(guān)。
結(jié)合上述分析繪制圖6,可以較形象的闡明IAS與3種表面活性劑間的協(xié)同作用機(jī)理。IAS單獨(dú)使用時(shí),緩蝕劑膜層存在大量的缺陷 (圖6a);當(dāng)IAS與DTAB復(fù)配使用時(shí) (圖6b),由于DTAB分子的空間位阻相對(duì)較小,其可以較充分的填充IAS膜層的缺陷,使得復(fù)合緩蝕劑的膜層更加致密;當(dāng)IAS與TTAB復(fù)配使用時(shí) (圖6c),TTAB分子的空間位阻比DTAB大,其填充缺陷的能力有限,使復(fù)合緩蝕劑膜層產(chǎn)生較大孔隙,導(dǎo)致TTAB與IAS間的協(xié)同作用程度較小;而當(dāng)IAS與CTAB復(fù)配時(shí) (圖6d),由于CTAB分子的空間位阻較大,其無法填補(bǔ)IAS膜層的缺陷,因此IAS與CTAB間不存在緩蝕協(xié)同效應(yīng)。此外,CTAB的緩蝕性能相對(duì)較好,其與IAS間可能還存在著競(jìng)爭(zhēng)吸附,這也可能是導(dǎo)致二者間產(chǎn)生拮抗效應(yīng)的原因。
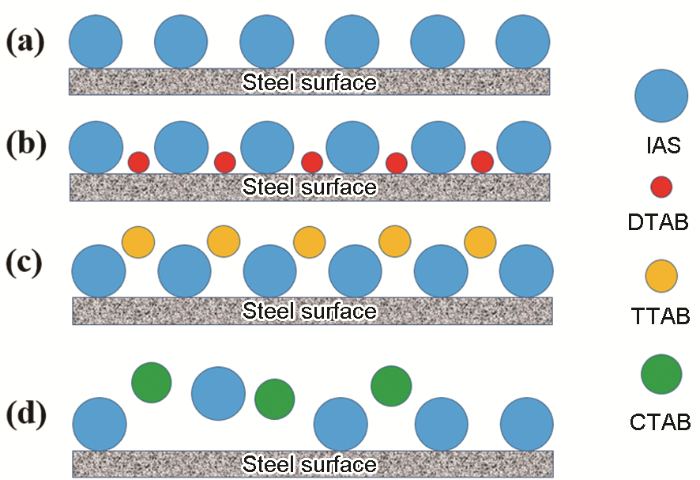
圖6 CO2/H2S共存鹽水溶液中IAS與3種表面活性劑在碳鋼表面的成膜機(jī)理示意圖
4 結(jié)論
(1) 在3種緩蝕劑復(fù)配體系中,復(fù)合緩蝕劑膜FFV值的降低程度與緩蝕協(xié)同效應(yīng)強(qiáng)度間具有一定的相關(guān)性,所得結(jié)論與課題組前期研究成果保持一致。
(2) IAS可有效抑制Q235鋼在含CO2/H2S鹽水溶液中的腐蝕;IAS與DTAB間存在較好的緩蝕協(xié)同效應(yīng),與TTAB間的協(xié)同作用較弱,而與CTAB間存在明顯的拮抗作用。
(3) IAS與3種表面活性劑形成的復(fù)合緩蝕劑均屬于以抑制陽極為主的混合型緩蝕劑。
(4) IAS與3種表面活性劑復(fù)配使用時(shí),起主要緩蝕作用的物質(zhì)可能為IAS,而表面活性劑則起到填補(bǔ)緩蝕劑膜層缺陷的作用。不同復(fù)配體系協(xié)同效應(yīng)的差異,可能與緩蝕劑分子的空間位阻有關(guān)。
參考文獻(xiàn)
[1] Li X H, Deng S D, Fu H, et al. Synergism between rare earth cerium (IV) ion and vanillin on the corrosion of cold rolled steel in 1.0 M HCl solution [J]. Corros. Sci., 2008, 50: 3599
doi: 10.1016/j.corsci.2008.09.029
[2] Oguzie E E, Li Y, Wang F H. Corrosion inhibition and adsorption behavior of methionine on mild steel in sulfuric acid and synergistic effect of iodide ion [J]. J. Colloid Interface Sci., 2007, 310: 90
doi: 10.1016/j.jcis.2007.01.038
[3] Okafor P C, Liu X, Zheng Y G. Corrosion inhibition of mild steel by ethylamino imidazoline derivative in CO2-saturated solution [J]. Corros. Sci., 2009, 51: 761
doi: 10.1016/j.corsci.2009.01.017
[4] Qiu L G, Wu Y, Wang Y M, et al. Synergistic effect between cationic gemini surfactant and chloride ion for the corrosion inhibition of steel in sulphuric acid [J]. Corros. Sci., 2008, 50: 576
doi: 10.1016/j.corsci.2007.07.010
[5] Okafor P C, Zheng Y G. Synergistic inhibition behaviour of methylbenzyl quaternary imidazoline derivative and iodide ions on mild steel in H2SO4 solutions [J]. Corros. Sci., 2009, 51: 850
doi: 10.1016/j.corsci.2009.01.027
[6] Li X H, Deng S D, Fu H, et al. Synergistic inhibition effects of bamboo leaf extract/major components and iodide ion on the corrosion of steel in H3PO4 solution [J]. Corros. Sci., 2014, 78: 29
doi: 10.1016/j.corsci.2013.08.025
[7] Khamis A, Saleh M M, Awad M I. Synergistic inhibitor effect of cetylpyridinium chloride and other halides on the corrosion of mild steel in 0.5 M H2SO4 [J]. Corros. Sci., 2013, 66: 343
doi: 10.1016/j.corsci.2012.09.040
[8] Zhao J M, Chen G H. The synergistic inhibition effect of oleic-based imidazoline and sodium benzoate on mild steel corrosion in a CO2-saturated brine solution [J]. Electrochim. Acta, 2012, 69: 247
doi: 10.1016/j.electacta.2012.02.101
[9] Zhang J, Sun X J, Ren Y M, et al. The synergistic effect between imidazoline-based dissymmetric bis-quaternary ammonium salts and thiourea against CO2 corrosion at high temperature [J]. J. Surfactants Deterg., 2015, 18: 981
doi: 10.1007/s11743-015-1744-0
[10] Zhang C, Zhao J M. Synergistic inhibition effect of imidazoline ammonium salt and three anionic surfactants in CO2-saturated brine solution [J]. J. Chin. Soc. Corros. Prot., 2015, 35: 496
[10] (張晨, 趙景茂. CO2飽和鹽水溶液中咪唑啉季銨鹽與3種陰離子表面活性劑之間的緩蝕協(xié)同效應(yīng) [J]. 中國(guó)腐蝕與防護(hù)學(xué)報(bào), 2015, 35: 496)
doi: 10.11902.1005.4537.2014.157
[11] Zhang C, Zhao J M. Synergistic inhibition effect of imidazoline ammonium salt and sodium dodecyl sulfate in CO2 system [J]. Acta Phys.-Chim. Sin., 2014, 30: 677
doi: 10.3866/PKU.WHXB201402111
[12] Amin M A, Mohsen Q, Hazzazi O A. Synergistic effect of I- ions on the corrosion inhibition of Al in 1.0 M phosphoric acid solutions by purine [J]. Mater. Chem. Phys., 2009, 114: 908
doi: 10.1016/j.matchemphys.2008.10.057
[13] Li X H, Deng S D, Fu H, et al. Synergistic inhibition effect of rare earth cerium (IV) ion and anionic surfactant on the corrosion of cold rolled steel in H2SO4 solution [J]. Corros. Sci., 2008, 50: 2635
doi: 10.1016/j.corsci.2008.06.026
[14] Obot I B, Obi-Egbedi N O, Umoren S A. The synergistic inhibitive effect and some quantum chemical parameters of 2,3-diaminonaphthalene and iodide ions on the hydrochloric acid corrosion of aluminium [J]. Corros. Sci., 2009, 51: 276
doi: 10.1016/j.corsci.2008.11.013
[15] Hao Y S, Sani L A, Ge T J, et al. The synergistic inhibition behaviour of tannic acid and iodide ions on mild steel in H2SO4 solutions [J]. Corros. Sci., 2017, 123: 158
doi: 10.1016/j.corsci.2017.05.001
[16] Musa A Y, Jalgham R T T, Mohamad A B. Molecular dynamic and quantum chemical calculations for phthalazine derivatives as corrosion inhibitors of mild steel in 1 M HCl [J]. Corros. Sci., 2012, 56: 176
doi: 10.1016/j.corsci.2011.12.005
[17] Wang D, Xiang B, Liang Y P, et al. Corrosion control of copper in 3.5wt.% NaCl solution by domperidone: Experimental and theoretical study [J]. Corros. Sci., 2014, 85: 77
doi: 10.1016/j.corsci.2014.04.002
[18] Yan Y G, Wang X, Zhang Y, et al. Molecular dynamics simulation of corrosive species diffusion in imidazoline inhibitor films with different alkyl chain length [J]. Corros. Sci., 2013, 73: 123
doi: 10.1016/j.corsci.2013.03.031
[19] Zhang J, Yu W Z, Yu L J, et al. Molecular dynamics simulation of corrosive particle diffusion in benzimidazole inhibitor films [J]. Corros. Sci., 2011, 53: 1331
[20] Qiang Y J, Zhang S T, Guo L, et al. Experimental and theoretical studies of four allyl imidazolium-based ionic liquids as green inhibitors for copper corrosion in sulfuric acid [J]. Corros. Sci., 2017, 119: 68
doi: 10.1016/j.corsci.2017.02.021
[21] Liao L L, Mo S, Luo H Q, et al. Relationship between inhibition performance of melamine derivatives and molecular structure for mild steel in acid solution [J]. Corros. Sci., 2017, 124: 167
doi: 10.1016/j.corsci.2017.05.020
[22] Salarvand Z, Amirnasr M, Talebian M, et al. Enhanced corrosion resistance of mild steel in 1 M HCl solution by trace amount of 2-phenyl-benzothiazole derivatives: Experimental, quantum chemical calculations and molecular dynamics (MD) simulation studies [J]. Corros. Sci., 2017, 114: 133
doi: 10.1016/j.corsci.2016.11.002
[23] Li X H, Deng S D, Lin T, et al. 2-Mercaptopyrimidine as an effective inhibitor for the corrosion of cold rolled steel in HNO3 solution [J]. Corros. Sci., 2017, 118: 202
doi: 10.1016/j.corsci.2017.02.011
[24] Zhang C, Zhao J M. Synergistic inhibition effects of octadecylamine and tetradecyl trimethyl ammonium bromide on carbon steel corrosion in the H2S and CO2 brine solution [J]. Corros. Sci., 2017, 126: 247
[25] Singh A, Lin Y H, Obot I B, et al. Macrocyclic inhibitor for corrosion of N80 steel in 3.5% NaCl solution saturated with CO2 [J]. J. Mol. Liq., 2016, 219: 865
doi: 10.1016/j.molliq.2016.04.048
[26] Ferreira E S, Giacomelli C, Giacomelli F C, et al. Evaluation of the inhibitor effect of L-ascorbic acid on the corrosion of mild steel [J]. Mater. Chem. Phys., 2004, 83: 129
[27] Yu Z J, Kang E T, Neoh K G. Electroless plating of copper on polyimide films modified by surface grafting of tertiary and quaternary amines polymers [J]. Polymer, 2002, 43: 4137
doi: 10.1016/S0032-3861(02)00263-X
[28] Xu J, Han X, Liu H L, et al. Synthesis and optical properties of silver nanoparticles stabilized by gemini surfactant [J]. Colloid. Surf. A, 2006, 273: 179
[29] Weng L T, Poleunis C, Bertrand P, et al. Sizing removal and functionalization of the carbon fiber surface studied by combined TOF SIMS and XPS [J]. J. Adhes. Sci. Technol., 1995, 9: 859
doi: 10.1163/156856195X00743
免責(zé)聲明:本網(wǎng)站所轉(zhuǎn)載的文字、圖片與視頻資料版權(quán)歸原創(chuàng)作者所有,如果涉及侵權(quán),請(qǐng)第一時(shí)間聯(lián)系本網(wǎng)刪除。
-
標(biāo)簽: CO2/H2S腐蝕, 碳鋼, 緩蝕劑, XPS, 分子動(dòng)力學(xué)模擬, 自由體積分?jǐn)?shù)

官方微信
《中國(guó)腐蝕與防護(hù)網(wǎng)電子期刊》征訂啟事
- 投稿聯(lián)系:編輯部
- 電話:010-62316606-806
- 郵箱:fsfhzy666@163.com
- 中國(guó)腐蝕與防護(hù)網(wǎng)官方QQ群:140808414





