摘要:
通過實驗室動態模擬給水實驗,研究了氧化還原電位 (ORP) 與溶氧量、pH值、溫度、流速的關系,并提出ORP經驗計算式。結果表明,水溶液體系ORP隨溶氧量的增大而增大,隨pH值及溫度的升高而減小,且受流速影響較小。相對于常溫ORP測量,高溫ORP信號有靈敏度高、精確性好的特點,能夠實現對痕量溶氧的有效測量。在電廠實際運行中,可根據高溫在線ORP監測結果,結合金屬電位-pH值圖判斷金屬腐蝕傾向,進而優化給水ORP。
關鍵詞: 氧化還原電位 ; 溶氧量 ; pH值 ; 20#碳鋼 ; 高溫給水環境
氧化還原電位 (ORP) 是指由貴金屬 (Pt或Au) 指示電極、標準參比電極和被測溶液組成的測量電池的電動勢[1],是溶液氧化性或還原性相對程度的表征。目前,國內電廠ORP測量主要應用于水的膜處理中加氯和除氯過程的監測,廢水處理中氧化性物質或還原性物質的識別。國外核電站則將其作為一種有效的水汽循環系統腐蝕監測手段,用于控制沸水堆 (BWR)、壓水堆 (PWR) 一回路的加氫水化學 (HWC) 和PWR二回路的加氧水化學[2,3,4]。特別是在HWC中,ORP可反映系統痕量O2和H2的相對含量,判斷蒸汽發生器等應力腐蝕開裂 (SCC) 易發部位的材料腐蝕傾向。在美國、日本等國家的火電廠中,通過對凝結水出口、除氧器進出口和省煤器入口等位點水樣進行原位ORP監測,采用PID自動控制氧化劑/還原劑的加藥量,控制凝結水-給水系統的腐蝕[5,6,7,8,9,10]。受限于高溫高壓在線ORP監測技術對電極材料要求嚴格、現有監測設備價格高昂等問題,該技術在國內電廠并未取得大規模的應用。
隨著我國火電的迅猛發展,高參數、大功率機組對汽水品質監督和金屬腐蝕監控也提出了更加嚴格的要求。目前,在給水水質監控中需要考慮pH值、O2、氫電導率等眾多參數,而這些參數并不能為運行人員提供直觀、全面的腐蝕控制全貌,如何通過水質監測指標正確反映熱力系統的腐蝕狀況并進行控制就顯得至關重要。高溫高壓在線ORP監測技術具有靈敏度高、響應迅速、無需降壓限流等特點,能夠實時獲取水汽循環系統水化學和腐蝕環境原位信息,了解金屬材料服役狀態、評估設備腐蝕風險、進一步實現水化學自動反饋控制,對電廠安全經濟運行有重要意義。因此,發展火電高溫高壓水環境ORP在線監測技術勢在必行。由于高溫高壓水的特殊環境,目前國內關于高溫ORP原位測量開展的研究工作較少,數據積累不足,還無法做到根據監測信號判斷發生的腐蝕類型,也無法實現對腐蝕過程的定量評價。本文通過實驗室模擬實驗,考查溶氧量 (DO)、pH值、流速、溫度等因素與ORP的關系,并采用電化學方法研究20#碳鋼在模擬給水環境下的腐蝕特性,分析ORP與金屬腐蝕的關系,為高溫高壓水環境ORP監測提供理論依據。
1 實驗方法
1.1 儀器及試劑
為模擬電廠給水管路實際運行環境,在實驗室中建立動態模擬裝置進行實驗。該裝置由溶液箱、循環泵、流量計、閥門、密閉測量池、加熱器、電極和測量儀表等組成,系統如圖1所示。模擬裝置最高工作壓力3 MPa,最高工作溫度150 ℃。實驗主要測量儀器為CST500型電位測定記錄儀,PHS-3C型pH計,哈希9582溶氧分析儀 (精度0.5 μg),CHI660D電化學工作站。常溫電極包括雷磁218型Ag/AgCl參比電極、10 mm×10 mm×0.2 mm Pt電極。高溫高壓電極為美國CORR儀器公司生產的外壓平衡式Ag/AgCl參比電極和Pt對電極,材質為C276合金。實驗用水為高純水 (18.25 MΩ·cm),因模擬水化學溶液為凈水體系,參比電極溶液均采用0.1 mol/L的KCl溶液。實驗所用主要試劑有KOH,KCl,HNO3,HCl,醌氫醌等 (分析純)。
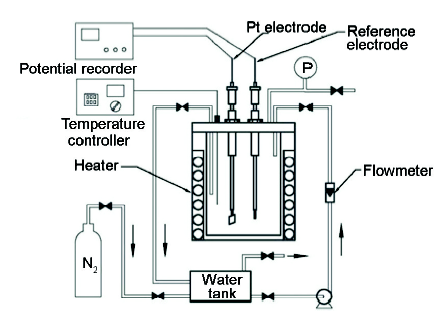
圖1 動態模擬測量試驗裝置
1.2 實驗步驟
實驗介質為實驗室配置的模擬不同給水化學工況溶液。因氨水具有易揮發性,通氮除氧過程對溶液pH值的精確控制有一定影響,本實驗采用NaOH作為溶液pH值調節堿化劑。
ORP測量實驗在模擬裝置中進行。實驗前,先將裝置及電極清洗干凈,固定安裝兩電極系統,并檢查裝置氣密性。電極的清洗及校正參照DL/T 1480。Pt電極依次使用硝酸 (質量分數約50%) 和水洗凈后,利用醌氫醌標準溶液校驗電極電位[11]。然后,將配置好的體積為2 L的溶液加入溶液箱,通入N2除氧,啟泵循環后利用溶氧儀進行測定,待溶氧穩定到期望值 (±2 μg/L) 后停止通氮。打開加熱器,加熱至設定恒溫 (±1 ℃)。實驗過程中,通過調節溶液箱出液口閥門的開度控制溶液循環流速。最后,待電位測定儀示值穩定后,讀取記錄溶液ORP值。同一條件下進行多次重復實驗,直至3次ORP測量示值偏差的絕對值不超過5 mV,取平均值記錄。所得ORP測量值與參比電極相對于氫電極的電位值之和即為標準電位E(SHE)。本文通過下式將所測高溫電位轉換為25 ℃下標準氫電極電位[12]:
E SHE = E obs + E ref + 3 × 10 - 6 × T - T 0 3 - 0.0025 × T - T 0 2 - 0.759 × T - T 0(1)
式中,ESHE為相對氫電極的氧化還原電位,mV;Eobs為所用參比電極實測的氧化還原電位,mV;Eref為所用參比電極25 ℃下相對氫電極的電位,mV;T為所測體系溫度,℃;T0為常溫 (25 ℃)。
選用爐前系統典型金屬材料20#碳鋼進行腐蝕實驗研究。將暴露面積為10 mm×10 mm的20#碳鋼工作電極固定安裝于圖1所示的密閉裝置,在模擬溶液環境下腐蝕40 d,每間隔1 d測量溶液ORP和碳鋼金屬電位 (ECP)。實驗環境溫度為恒溫80 ℃,初始pH值9.0,DO100 μg/L,流速100 mL/min。
2 結果與討論
2.1 ORP影響因素考查
火電廠給水中存在多個氧化還原過程,如O2/OH-,Fe/Fe3+等,但由于給水水質受到了嚴格控制,氫電導率不超過0.15 μS/cm,Fe2+含量也低于10 μg/L。其它電對的氧化還原過程相對于O2/OH-很弱,在給水中對ORP的影響較小。水的ORP測量影響因素除了DO外,主要有pH值、溫度、各電對反應性質和電極表面狀態等[13,14]。本文主要研究了DO、pH值、溫度和流速對ORP的影響。
2.1.1 溶解氧濃度與ORP關系 根據電廠水汽取樣分析裝置主要技術指標,選取溫度為25,35和45 ℃,流速為500 mL/min,模擬常規汽水取樣條件下ORP監測情況。測得pH值為 (9.00±0.05) 的NaOH溶液的ORP隨DO變化如圖2所示。由圖可見,ORP隨溶解氧濃度的增大呈現正向增大的趨勢。結果符合O2/OH-電對的Nernst方程,O2為氧化性物質,其濃度越大ORP越正。分析圖2可知,在3個不同溫度下,ORP隨DO變化趨勢一致,在DO為0~0.5 mg/L的低濃度范圍內,ORP隨DO增大而迅速增大。當DO大于1.0 mg/L時,ORP增加幅度減小。
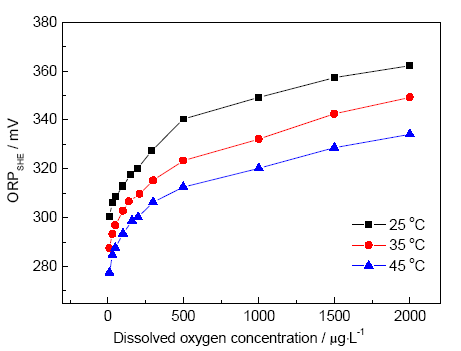
圖2 不同溫度下ORP隨DO變化曲線
圖3是ORP隨lgDO的變化曲線。對25 ℃下測量結果作線性擬合,在DO為0~0.5 mg/L的范圍內,曲線滿足ESHE=283.14+15.78 lgDO的函數關系,相關系數R2為0.9884。由此可見,在低氧濃度下,ORP與lgDO有一定的線性關系。在模擬溶液中,Na+不參與氧化還原過程,氧化還原電對O2/OH-參與的平衡反應為:
O 2 ( g ) + 2 H 2 O ( l ) + 4 e -
其ORP的大小遵循Nernst方程,可得O2/OH-平衡電位的計算公式:
E m = E O 2 O H - θ + 2.303 RT 4 F × lg p ( O 2 ) p θ - 2.303 RT F × pH + 0.8288(3)
式中,Em為氧化還原電位,V;Eθ為標準電極電位,V;R為氣體常數,8.314 J·mol-1·K-1;T為熱力學溫度,K;F為Faraday常數,9.64845×104 C·mol-1; p ( O 2 ) 為氧的絕對壓力,kPa;pθ為標準大氣壓,101.325 kPa。
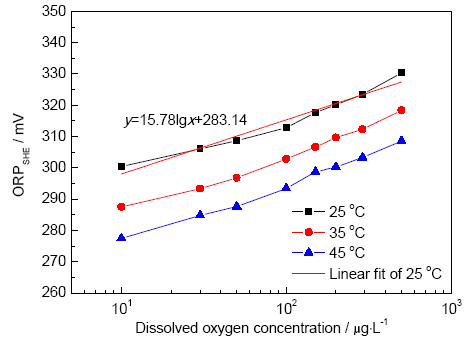
圖3 不同溫度下ORP與lgDO的關系
根據Henry定律,在稀溶液中,O2在液面上的分壓力可用下式求得:
p B = k c , b × c B(4)
式中,PB為該氣體B在液面上的分壓力,kPa;kc,b為Henry定律常數;cB為氣體的物質的量濃度,mol/m3。
25 ℃下, E O 2 O H - θ =0.4009 V,kc,B=7.8532×10-1 atm·mol-1·m3。帶入式 (4),計算得:
E O 2 O H - = 1160.6 + 14.8 lgDO - 59.2 pH(5)
將本實驗條件pH值為9.0代入式 (5),得 E O 2 O H - =627.8+14.8 lgDO。其中,DO單位為μg/L; E O 2 O H - 為電位,mV。由式 (5) 可知,在DO低于0.5 mg/L條件下,理論計算式與實驗擬合式中lgDO項的系數大致吻合。但同一溶氧濃度下,水溶液ORP實際測量值遠低于理論計算值,如DO為100 μg/L時,ORP測量值為315 mV,計算值為657 mV,相差342 mV。黃茜等[15]認為在貴金屬電極表面上的O2/OH-反應是一個極為緩慢的反應,即使在溶氧達到飽和的情況下,ORP也難以達到O2/OH-的平衡電位,因此,測量值遠低于計算值。Macdonald[3]研究表明,在275 ℃下模擬BWR水化學溶液中,只有在高堿性 (0.1 mol/L LiOH,pH值為10.45),[O2]≥7 mg/L的條件下,ORP測量值與計算值有良好的一致性,其它情況下都要遠遠小于理論值,差值約為300 mV。其認為一方面是由于Pt電極存在極微弱的O2的氧化污染,測得電位為Pt的氧化與O2的還原過程的混合電位。另一方面,隨著水環境pH值及O2濃度的增大,氧氣還原反應中正逆反應的交換電流密度增大,而Pt電極氧化過程交換電流密度極小,所以氧氣電極反應的可逆程度增大,ORP測量值越接近平衡電位。Hoare[16]也指出,在含氧體系中Pt電極不是完全惰性的,在其表面會有極其微弱、緩慢的Pt氧化過程的發生。
模擬火電廠低壓加熱器典型溫度和水化學環境,在80,100,120 ℃下進行ORP測量,所得pH值為9.0的NaOH溶液ORP隨DO變化關系曲線如圖4所示。可以看出,高溫下ORP與溶氧濃度的對數也呈正相關的關系。表1列出了ORP與lgDO的線性擬合式與其相關系數R 2。在0~1 mg/L的溶氧濃度范圍內,ORP隨著溫度的升高而降低,且隨著溫度的升高,曲線斜率正向增大。結合式 (5) Nernst方程可知,系數RT/nF決定了ORP-lgDO的斜率,溫度越高,斜率越大,測量結果與理論預測一致。由于缺少部分高溫電極過程動力學基礎參數,對高溫ORP進行精確計算存在一定困難。與本實驗結果類似的,Niedrach等[17]也研究得到了高溫下電位與lgDO的線性經驗擬合式,證明DO在一定濃度范圍條件下,ORP與lgDO可用線性關系式表達。對比高溫與常溫測量結果,高溫下ORP對痕量溶氧的變化波動更大,如10~100 μg/L的DO變化,對應常溫下ORP波動為16 mV,100 ℃下為76 mV,波動明顯。近年來,國內電廠已多次發生因氧化皮剝落、堆積、堵塞造成爆管等事故[18],過熱器和再熱器蒸汽側氧化皮生成與剝落問題受到重視。作為可能的影響因素之一,給水和蒸汽DO應受到更加嚴格地監控[19,20],高溫ORP在線測量無疑為痕量DO的精確控制提供了一種可行方案。

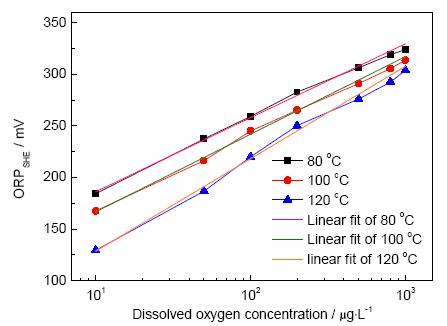
圖4 高溫條件下ORP與氧含量對數的關系
2.1.2 pH值與ORP關系 圖5為25 ℃,500 mL/min流速下,ORP隨pH值變化關系曲線。可見,ORP隨pH值的增大而逐漸減小。實驗結果符合Nernst電位理論,即氧化還原電位通常隨著H+活度的增加而增大,隨著OH-活度的增加而減小。實驗測得在25 ℃下,ORP與pH值線性關系明顯,pH值每升高一個單位,ORP降幅約為52 mV。對比式 (5),理論上pH值每增加一個單位,ORP下降59.2 mV,實驗結果與理論計算相差不大。
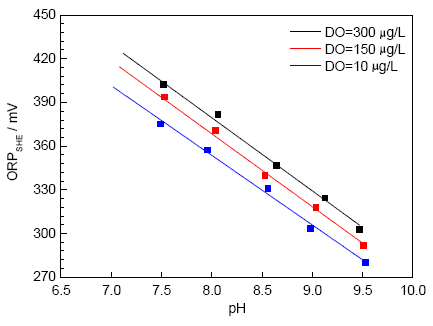
圖5 常溫下ORP與pH值的關系
實驗考查了不同溫度下ORP與pH值的變化關系,結果如圖6所示,擬合式列于表2。可以看出,ORP與pH值變化呈負相關,且具有線性關系。事實上,pH值測量的本質就為H+作用下的電位測量,一定溫度下,pH值與對應的電位值可轉換成線性關系。對比圖5,pH值每增大1個單位,高溫下ORP的降幅遠大于常溫測量結果,其主要是因為ORP受到了溫度變化的影響。根據式 (3),ORP-pH曲線的斜率為 - 2.303 RT F ? p H ( T ) p H ( 25 °C ) ,高溫pH(T ) 對pH(25 ℃) 有下式所示的近似換算關系:
pK w ( 25 °C ) pK w ( T ) = p H ( 25 °C ) p H ( T )(6)
式中,pKw為水的離子積的負對數。計算得100 ℃下,直線理論斜率為-64 mV/pH,實驗結果為-71 mV/pH。所以,在溫度一定,DO極低的條件下,ORP可反映pH值的大小。在火電廠實際給水pH值控制中,pH值波動范圍一般不會超過0.5,但高溫下ORP對pH值波動的響應是十分明顯的。在溶氧和pH值都波動較大的高溫環境下,可采用常溫pH值表輔助測量,以明確是否因DO波動而造成電位大幅度變化。
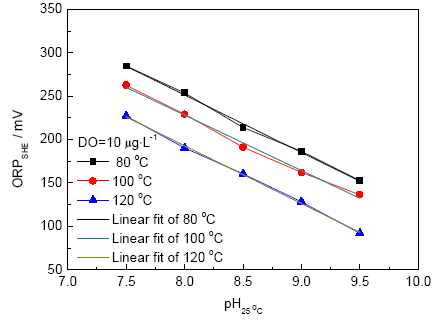
圖6 高溫下ORP與pH值的關系
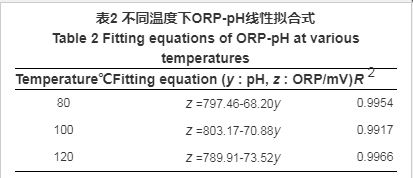
表2 不同溫度下ORP-pH線性擬合式
2.1.3 水樣流速與ORP關系 根據火電廠汽水取樣測量裝置中水樣流量一般控制在0~1000 mL/min,考察80 ℃下水樣流量對ORP的影響,結果如圖7所示。在較低的溶氧濃度下,水樣流量變化對ORP造成了輕微的波動,ORP隨水流量的增大而正向增加;在較高的溶氧濃度下,水樣流量對ORP無影響。Chen等[21]研究表明,受流體動力學條件對金屬表面電化學反應極限電流大小的影響,金屬電極電位也隨流體條件的改變而變化,包括線性流速、雷諾數Re、流體運動粘度、流通直徑等。在極低的氧濃度條件下,由于氧的還原為擴散步驟控制的電極過程,反應粒子自溶液本體向電極表面遷移擴散的傳質速率取決于流體動力學條件。增加流速降低了擴散層的厚度,增大了傳質速率,加速了金屬表面物質 (特別是氧化劑) 的電化學反應,導致電位的增大。流速對電位的影響是存在一定爭議的,Macdonald等[22]和Eason等[23]則認為流速對電位并沒有明顯的影響。在本實驗結果中,水流速對痕量溶氧下的水溶液ORP測量只有輕微影響。但在電廠其它ORP儀表使用環境中,如對加氯和除氯過程監測,氧化還原反應過程、ORP測量值與流體動力學條件的關系仍有待研究。考慮到ORP很難用計算方法加以校正,在實際測量中應當預先選定恰當的水樣流速范圍。
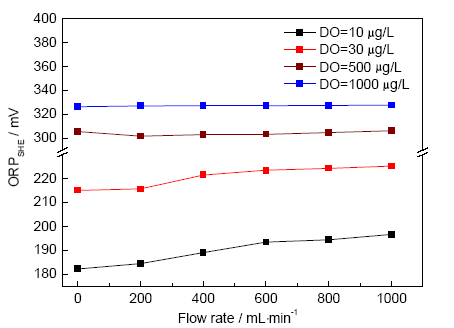
圖7 80 ℃下ORP隨水樣流量變化趨勢圖
2.1.4 溫度與ORP關系 圖8是ORP隨溫度的變化曲線。可見,ORP隨溫度的升高而逐漸降低。溫度不僅影響Nerest方程中的T,還可以影響電子轉移數和氧化劑還原劑濃度,從而也影響對數項的大小。同時,氧化還原電對O2/OH-電極反應的標準電極電勢也隨溫度的升高而降低,且并非遵從簡單的線性關系[24]。所以,ORP的測量值難以進行溫度補償,應避免被測體系溫度有較大的波動。
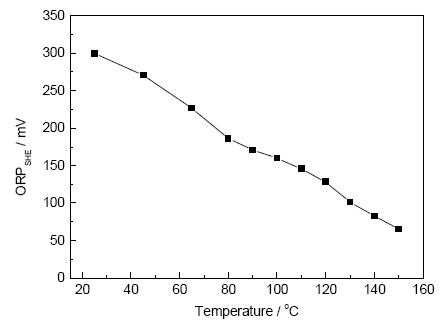
圖8 ORP與溫度的關系
2.2 ORP經驗擬合式
根據式 (3),在一定溫度下,ORP與lgDO、pH值符合簡單的二元一次方程。由表1和2擬合式,利用Mathmatica軟件得三者關系如圖9所示。在pH值為7~9.5,溶氧濃度為0~1 mg/L的范圍內,本實驗所得ORP經驗擬合式列于表3。
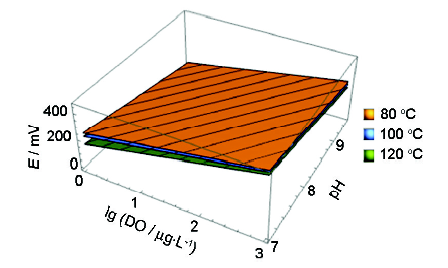
圖9 不同溫度下ORP與DO、pH值的關系
表3 不同溫度下ORP-DO-pH線性擬合式

為檢驗計算式是否與實驗結果具有良好的一致性,利用SPSS軟件中Wilcoxon檢驗模塊對不同條件下ORP的計算值與測量值進行兩配對樣本的非參數檢驗。此檢驗方法是在數據總體分布不甚了解的情況下,通過兩組配對樣本的分析,推斷樣本來自的兩個總體的分布是否存在顯著性差異的方法。
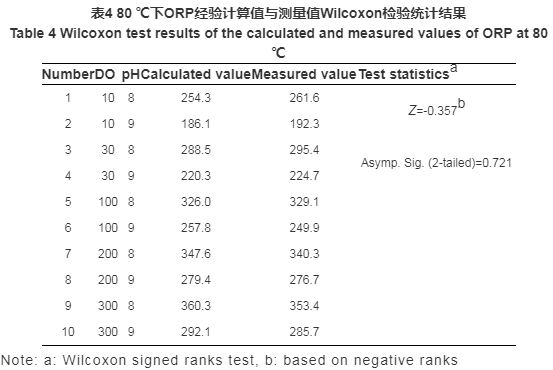
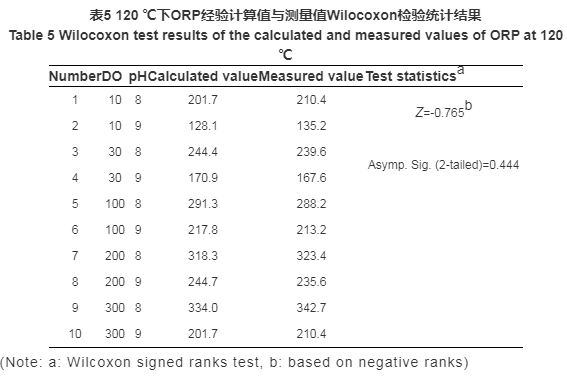
實驗中采用Wilcoxon檢驗模塊對ORP計算值與測量值配對進行檢驗,并輸出描述性統計量。原假設為,ORP實驗測量值與經驗計算值無顯著差異。秩和檢驗的結果如表4和5所示,表中給出的是Z統計數和近似的p值。80 ℃下,漸進顯著性 (雙側) 為0.721,說明概率p值為0.721,遠大于顯著性水平0.05,因此,原假設成立。同理,150 ℃下原假設也成立。可見ORP經驗計算式所得結果與實驗測量值的差異并無統計學顯著性意義,二者具有一致性,即可根據經驗計算式對ORP值進行計算與預測。
2.3 ORP與金屬腐蝕的關系
在金屬腐蝕過程中,電位是金屬陽極溶解過程的控制因素,溶液的pH值則是金屬腐蝕產物穩定性的控制因素[25]。應用這兩個參數,可把金屬-水溶液體系中各個反應在給定條件下的平衡關系用電位-pH平衡圖表示,進而了解金屬腐蝕的可能性和腐蝕產物的穩定性,為電廠水化學工況的調節與優化提供依據。采用熱力學軟件HSC Chemistry繪制電位-pH圖見圖10和11。平衡計算中有關離子的濃度均取10-6 mol/L,H2和O2的分壓為標準壓力 (100 kPa)。根據圖10中不同區域物質的穩定存在狀態,可劃分為Fe的免蝕區、腐蝕區和鈍化區。由先前實驗結果可知,在80 ℃,pH值為9.0,DO>10 μg/L的條件下,給水環境ORP>170 mV,對應圖中區域為Fe2O3的熱力學穩定區,Fe表面上可能形成完整、致密的氧化物保護膜,從而抑制其溶解,降低腐蝕速率。而對于Cu-H2O體系,相同pH值、ORP條件下,對應圖11中Cu2O或Cu(OH)2的熱力學穩定區,在氨存在的條件下易發生氨腐蝕,進而引發Cu的遷移與沉積。因此,在凝結水-給水系統含銅合金的電廠中一般采用還原性全揮發處理,加入還原劑聯胺使給水ORP<-200 mV。所以,將ORP測量值與體系pH值結合起來,利用金屬電位-pH圖能夠判斷鍋爐機組水化學調節方式是否合理。
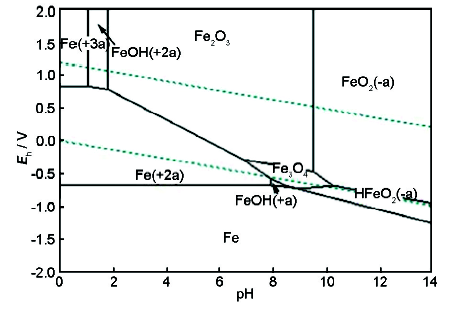
圖10 80 ℃下Fe-H2O體系電位-pH圖
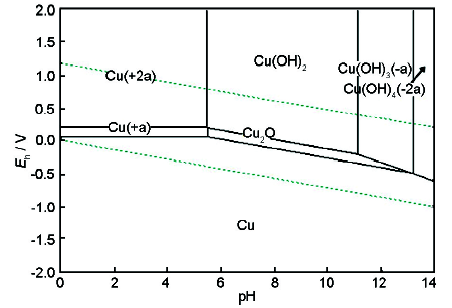
圖11 80 ℃下Cu-H2O體系電位-pH圖
腐蝕實驗測得20#碳鋼腐蝕電位與溶液ORP的關系如圖12所示。可見,金屬腐蝕電位先逐漸增大,在18 d后電位逐漸穩定。ORP則逐漸減小,在碳鋼腐蝕電位穩定后ORP也趨于穩定。可見,碳鋼在高ORP、高pH值條件下逐漸發生鈍化,腐蝕生成的Fe3O4或Fe2O3覆蓋在金屬基體表面,形成氧化物保護膜,導致金屬電位的增大。當保護膜趨于完整時,金屬腐蝕速率降低,金屬電位也逐漸穩定。隨著金屬的氧化和溶氧的消耗,密閉環境中溶液的ORP逐漸降低。
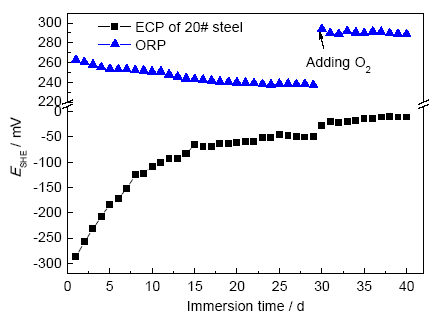
圖12 20#碳鋼腐蝕電位與溶液ORP關系圖
為探究ORP與ECP的相關性,第30 d通入O2進行擾動實驗。溶氧增大到500 μg/L后,ORP與ECP都立即正向增大,隨后ORP趨于穩定,ECP則繼續緩慢增大。這是因為雖然腐蝕電位和ORP是以類似的方式測量,但前者反映的是發生在金屬表面上的腐蝕反應。當金屬電極表面形成完整的鈍化膜后,金屬氧化腐蝕的速率極低,與惰性電極類似,金屬氧化膜表面提供了氧化還原電對反應的場所。所以,此時ECP與ORP的變化是一致的,但ORP更為靈敏,且一般大于金屬腐蝕電位。
3 結論
(1) 水溶液體系ORP隨DO的增大而增大,隨pH值的增大而減小,且與二者都具有一定的線性關系。ORP隨溫度的升高而降低,但其影響機理復雜,難以進行溫度補償。ORP受溶液流速影響較小。
(2) 提出了ORP在80和120 ℃下的經驗計算式,并采用Wilcoxon檢驗進行驗證,該計算式與實驗結果具有良好的一致性。
(3) 鈍化后的20#碳鋼的金屬電位與ORP變化趨勢一致,但無簡單的定量關系。將來仍需深入研究ORP信號與不同金屬的腐蝕過程及腐蝕機理之間的對應關系,現階段可根據金屬電位-pH圖判斷金屬腐蝕傾向,通過調節DO、pH值等水化學參數優化給水ORP。
免責聲明:本網站所轉載的文字、圖片與視頻資料版權歸原創作者所有,如果涉及侵權,請第一時間聯系本網刪除。

官方微信
《中國腐蝕與防護網電子期刊》征訂啟事
- 投稿聯系:編輯部
- 電話:010-62316606-806
- 郵箱:fsfhzy666@163.com
- 中國腐蝕與防護網官方QQ群:140808414





