軟組織具有高斷裂韌性,然而其力學機制尚不清晰。近日,西安交通大學唐敬達教授與哈佛大學鎖志剛教授合作,圍繞“膠原軟組織的增韌機制”開展研究,通過力學實驗與顯微觀測,得到了軟組織的牽引-分離定律,揭示了膠原軟組織高斷裂韌性的微觀機制,對仿生軟材料的設計具有指導意義。相關成果以Why are soft collagenous tissues so tough?為題,發表在國際期刊《Science Advances》上,并得到期刊主頁推薦。
右下為Sci. Adv. 期刊推薦的本文圖片
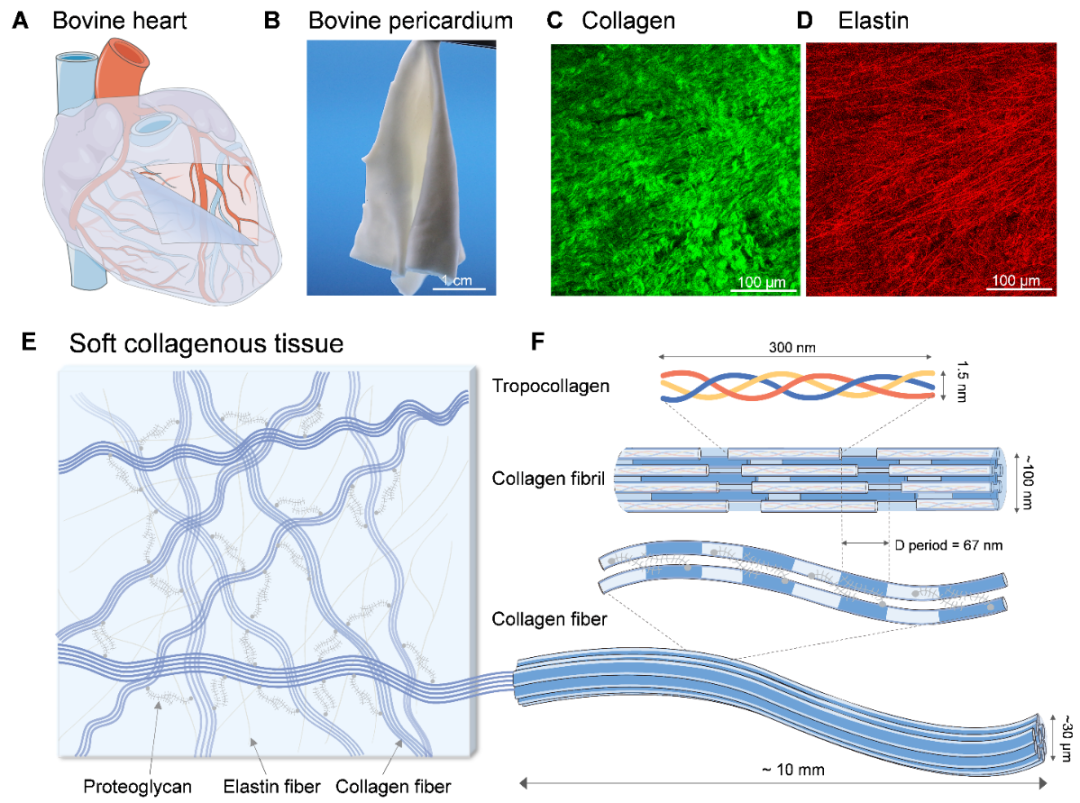
膠原軟組織,如皮膚、肌腱和心臟瓣膜,通常具有較高的斷裂韌性。例如,牛心包這種膠原軟組織用于人類心臟瓣膜置換手術,能承受數億次開閉循環而不開裂(圖1A,B)。本研究選取牛心包作為研究對象,探討了膠原軟組織的增韌機制。膠原軟組織的微觀結構如圖1C-F所示。
圖1.膠原軟組織微觀結構
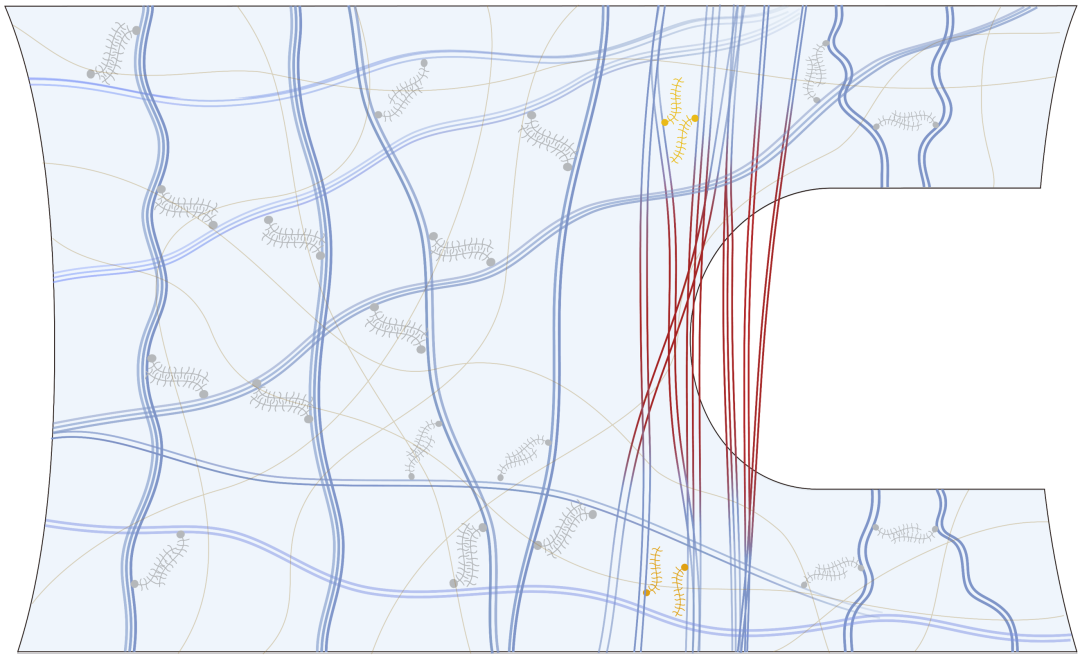
當裂紋在膠原軟組織中擴展時,膠原纖維在裂尖解卷曲,沿拉伸方向重新定向,從裂紋表面抽出形成橋接區阻礙裂紋擴展(圖2),該橋接過程可通過斷裂力學中的牽引-分離曲線(traction-separation curve)描述。
圖2.膠原纖維橋接裂紋
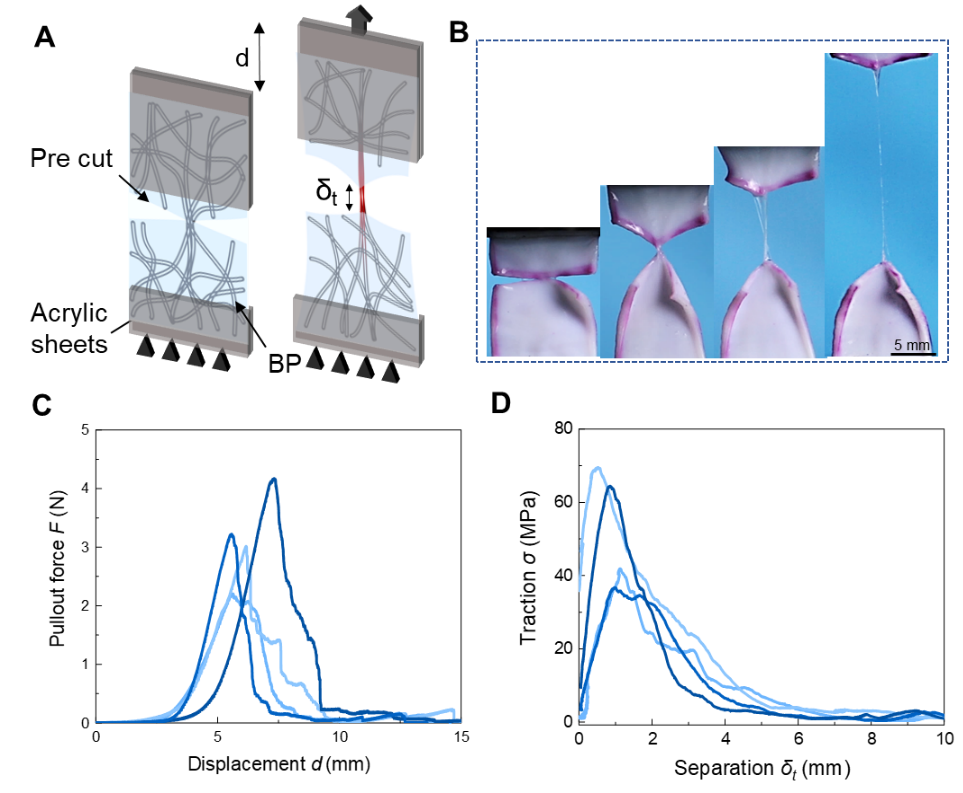
研究人員設計了“纖維抽出試驗”與“裂紋擴展試驗”兩種方法,測得了膠原組織的牽引-分離關系曲線。纖維抽出實驗中,在樣品兩側分別裁切預置裂紋,僅留下寬度約為300 µm的膠原纖維束(圖3A,B),然后直接從基質中抽出膠原纖維,記錄其抽出過程中的力-位移曲線,進而獲得牽引分離曲線。結果顯示,牛心包組織的峰值牽引應力約為60 MPa,最大裂紋分離長度約為6 mm(圖3C,D)。
圖3.膠原纖維抽出實驗
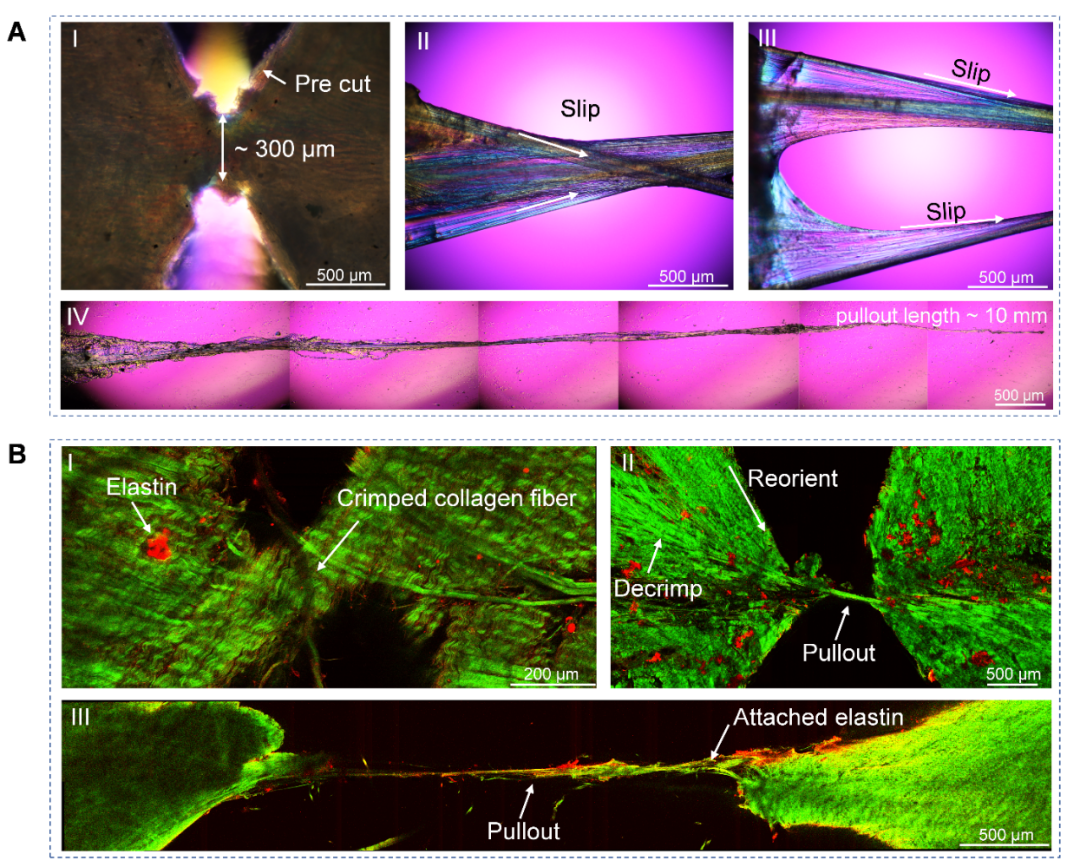
為了探明纖維抽出過程中的微觀機制,研究人員使用偏振光顯微鏡(圖4A)和雙光子顯微鏡(圖4B)記錄了膠原纖維在拉伸過程中不同階段的形貌變化。未變形時,卷曲的膠原纖維嵌入在彈性蛋白網絡中。抽出過程中,膠原纖維開始解卷曲,并沿拉伸方向重新定向,膠原纖維逐步被抽出,最終約10mm長的膠原纖維被完全抽出。
圖4.膠原纖維抽出過程中的微觀形貌變化
隨后,研究人員基于裂紋擴展過程中能量釋放率與牽引分離曲線的關系,設計“裂紋擴展實驗”測量了膠原軟組織的牽引分離曲線。首先觀察了裂紋擴展過程中,膠原纖維在裂尖的行為和微觀形貌變化。結果顯示,在未變形的樣品中,裂紋尖端保持完整,纖維呈卷曲狀(圖5A)。隨著拉伸比的增加,裂紋鈍化,卷曲的膠原纖維束拉直并沿拉伸方向重新取向(圖5B)。隨著進一步拉伸,裂紋開始在軟基體中擴展,膠原纖維被拉出并橋接裂紋,在裂紋尖端形成一個明顯的橋接區(圖5C)。
圖5.裂尖膠原纖維在擴展過程中的形貌變化
隨后,研究人員準備了預切裂紋的矩形樣品,對樣品進行拉伸(圖6A,B),使用黑色標記點對裂紋尖端的表面進行標記(圖6C)。研究人員根據裂紋尖端標記點的狀態和裂紋擴展進程,識別出膠原軟組織具有兩個特征能量釋放率值:GA和GB。實驗結果顯示,牛心包的兩個特征能量釋放率GA = 16.2 kJ/m2,GB = 112.1 kJ/m2。峰值牽引力σ0約為60.9 MPa。最大分離長度δ0約為4.8 mm(圖6D,E)。研究人員還研究了軟組織的牽引分離曲線隨樣品高度、纖維取向和含水量的變化。
圖6.裂紋擴展實驗
研究人員將膠原軟組織的牽引分離曲線與一些經典材料進行比較。軟組織的峰值牽引力約為60 MPa,接近骨骼、珍珠層和魚鱗片等,遠高于單向纖維/環氧樹脂復合材料。軟組織的最大分離長度約為6 mm,高于合成材料。由于膠原軟組織與硬組織的牽引力相當,而裂紋分離長度遠高于硬組織的,因此,膠原軟組織的斷裂韌性比硬生物組織高1~2個數量級(圖7A)。長膠原纖維從軟組織裂紋表面抽出形成較大尺寸的橋接區,提供高橋接應力,有效阻礙裂紋擴展,導致了軟組織的高斷裂韌性和裂紋不敏感性(圖7B)。最后比較了幾種經典材料的裂紋橋接機制(圖7C)。
圖7.膠原軟組織的增韌機制
該項工作揭示了膠原軟組織高斷裂韌性的力學機制,量化了裂紋橋接的牽引-分離關系,為開發仿生材料(如人造心臟瓣膜)提供了理論依據。
上述研究得到了國家優秀青年基金的資助,特別致謝上海紐脈醫療科技股份有限公司提供的牛心包樣品。
論文第一作者為西安交大碩士生唐婧嫄、通訊作者為西安交大唐敬達教授和哈佛大學鎖志剛教授,論文作者還包括西安交大博士生陳曦、劉豐愷,畢業碩士曾梁松(現為美國西北大學博士生)。
論文鏈接
https://www.science.org/doi/10.1126/sciadv.adw0808
免責聲明:本網站所轉載的文字、圖片與視頻資料版權歸原創作者所有,如果涉及侵權,請第一時間聯系本網刪除。

官方微信
《腐蝕與防護網電子期刊》征訂啟事
- 投稿聯系:編輯部
- 電話:010-62316606
- 郵箱:fsfhzy666@163.com
- 腐蝕與防護網官方QQ群:140808414